在哺乳动物生命发育的起点,受精卵与二细胞(2C)胚胎阶段,细胞拥有发育成完整个体的“全能潜能”,这是生命最特殊的“潜能巅峰”时期。但长期以来,发育生物学界有个关键难题悬而未决:胚胎如何精准“按时退出”全能态、启动分化并顺利着床?尤其是小鼠胚胎中,维持全能态的“2C 转录本”(如 Zscan4 基因、MERVL 逆转录转座子),必须在2C阶段后快速沉默,否则会阻断发育——而这一“转录终止”的调控机制,此前始终是未解之谜。前期研究已经发现,溶酶体在2C胚胎发育中具有重要作用。然而,由于全能胚胎样本获取难度高、单样本代谢物含量极低,传统代谢组学手段已经无法满足微量样本代谢物的检测工作,这也是长期制约全能胚胎中溶酶体信号转导的功能深入解析的关键障碍。
2024年10月28日,浙江大学傅旭东研究员团队在Developmental Cell杂志上发表题为“Lysosomal catabolic activity promotes the exit of murine totipotent 2-cell state by silencing early-embryonic retrotransposons”的文章,揭示了溶酶体代谢在2C阶段退出与抑制2C转录本表达中起到重要作用。这一发现揭示了一种新型的溶酶体信号转导对早期胚胎逆转录转座子的调控作用,建立了胚胎着床前发育过程中溶酶体信号转导和转录重塑之间的关联。其中,研究团队凭借微量样本代谢组学技术突破“全能胚胎样本量少、难检测”的瓶颈,为研究提供了关键数据支撑。

核心发现-01
溶酶体活性通过调节胞内氨基酸
水平抑制胚胎退出2C阶段
研究团队利用多西环素(Dux)诱导的全能样细胞(2CLC)模型研究溶酶体活性在胚胎早期发育中的作用。研究发现,全能态细胞(2CLC)的溶酶体活性,远低于分化后的多能态细胞(mESC):用溶酶体抑制剂(如Vacuolin-1、羟氯喹)处理后,mESC更易转化为全能态,且全能态维持时间更长——这说明,溶酶体活性低则“留住”全能态,活性高则“推动”全能态退出。
若想深入解析溶酶体在胚胎全能态调控中的具体作用机制,核心前提是精准捕捉全能胚胎(如2细胞胚胎)的代谢动态变化 —— 但这类胚胎样本量极小,传统代谢检测方法根本无法实现有效检测。于是,研究团队联合科似海生物构建了微量靶向代谢组学检测方法,精准解决了这一难题:通过定制化样本前处理与超灵敏检测技术,成功量化了微量全能胚胎中的氨基酸浓度,发现了关键规律:(1)溶酶体活性高时,胞内氨基酸浓度显著上升;(2)氨基酸饥饿会促进细胞进入全能态,而额外补充氨基酸,能直接抵消溶酶体抑制剂对全能态的“促进作用”。充分说明了溶酶体是通过调控胞内氨基酸水平,间接影响全能态转化的。(图1)。
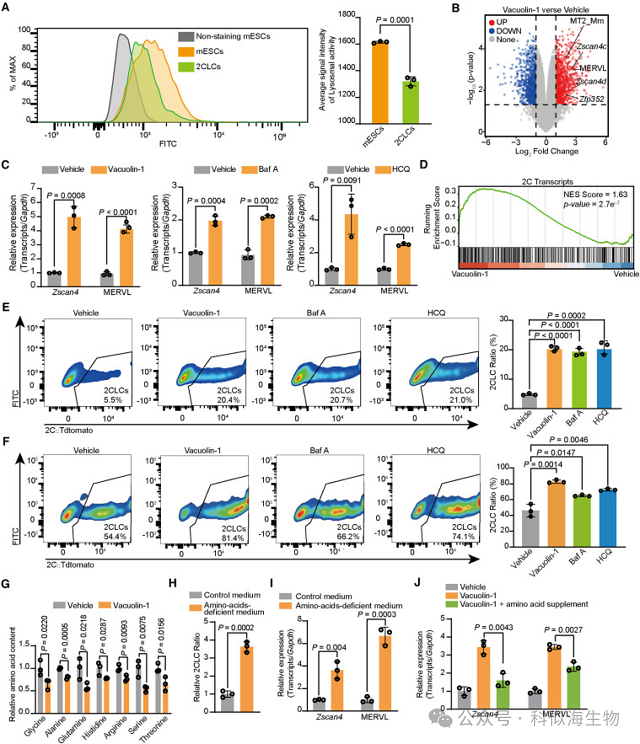
图1
核心发现-02
溶酶体活性通过激活RagC/D
使TFEB/TFE3失活来抑制2C样转变
氨基酸浓度变化后,信号如何传递到“2C 转录本”?研究进一步发现:氨基酸上升会激活溶酶体膜上的RagC/D蛋白。激活的RagC/D会招募转录因子 TFEB/TFE3,使其进入细胞质失活。如果敲除Flcn基因导致RagC/D 失活,TFEB/TFE3 会进入细胞核,直接激活“2C 转录本”(尤其是MERVL逆转录转座子)。(图2)。
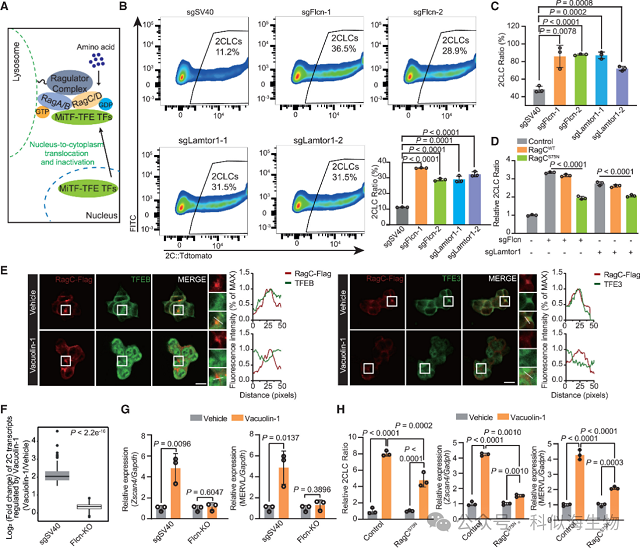
图2
核心发现-03
TFEB/TFE3直接结合并激活
MERVL/MT2_Mm维持全能态
过表达核定位的活性形式TFEB或TFE3,可显著促进mESC向2CLC转化,并上调逆转录转座子亚家族MERVL/MT2_Mm的表达;反之,敲除Tfeb/TFE3则会削弱溶酶体抑制剂对全能态的促进作用。通过CUT&Tag测序发现,在全能态下,TFEB/TFE3会特异性结合到MERVL/MT2_Mm的长末端重复序列(LTR)区域;进一步通过荧光素酶报告实验证实,TFEB/TFE3通过结合MERVL/MT2_Mm LTR中的第二段CLEAR基序,直接激活这些逆转录转座子的转录。MERVL/MT2_Mm作为2C胚胎中的“替代启动子”,可调控邻近2C基因(如Zscan4)的表达;TFEB/TFE3通过激活MERVL/MT2_Mm,间接上调下游2C基因表达,从而维持全能态;若MERVL/MT2_Mm的转录被抑制,TFEB/TFE3则无法激活2C基因,这证明MERVL/MT2_Mm是TFEB/TFE3调控全能态的核心靶点 (图3)。
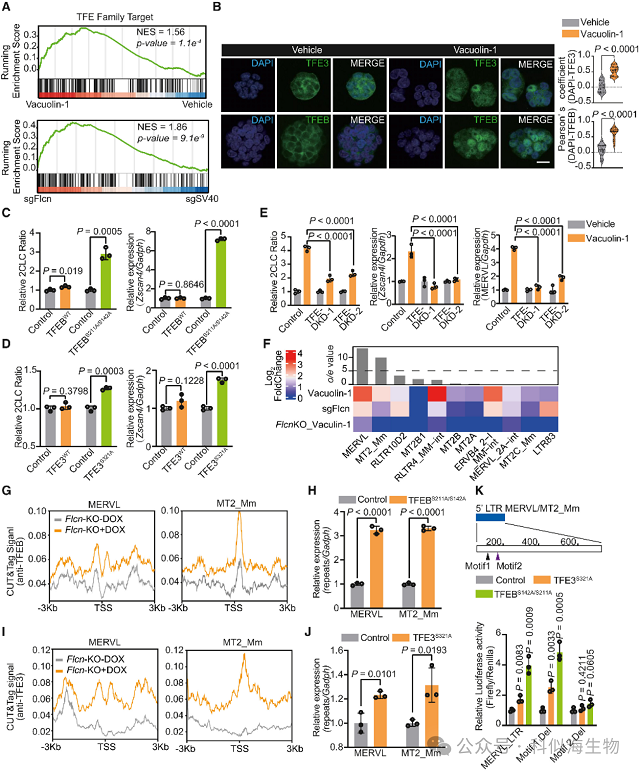
图3
核心发现-04
酶体信号通过沉默MERVL/MT2_Mm
推动全能态退出
结合以上发现,一条清晰的 “发育调控路径” 终于浮现:
2C 胚胎早期:溶酶体活性低→氨基酸少→RagC/D 失活→TFEB/TFE3 入核→激活 MERVL 与 2C 基因→维持全能态;
2C 胚胎晚期:溶酶体活性升高→氨基酸增加→RagC/D 激活→TFEB/TFE3 失活→MERVL 沉默→2C 基因下调→胚胎退出全能态,启动分化。(图4)。
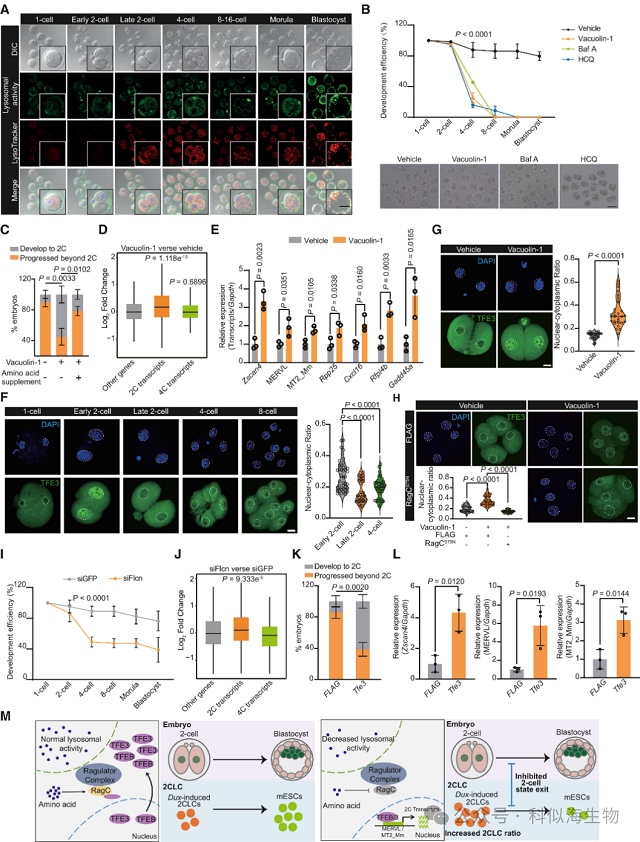
图4
文章总结
在本研究中,研究团队利用2CLC模型与小鼠胚胎,深入探究了溶酶体在胚胎早期发育中的作用。针对“全能胚胎样本量少、难以检测”的瓶颈,研究团队构建微量样本代谢组学检测方法,实现对微量胚胎样本中溶酶体氨基酸含量的精准监测,为解析溶酶体信号转导功能提供数据支撑。研究发现溶酶体的分解代谢活性通过“溶酶体活性→胞内氨基酸→RagC/D→TFEB/TFE3→2C转录本(MERVL/MT2_Mm)”的信号通路,抑制2C转录本表达,最终推动小鼠全能2C胚胎退出全能态、启动后续发育。该研究首次揭示溶酶体信号转导对早期胚胎逆转录转座子的调控作用,建立“胚胎着床前发育中溶酶体信号转导与转录重塑”的关联,为理解胚胎早期全能态调控网络提供了全新视角。
在本研究中,杭州科似海生物科技有限公司提供了全能胚胎样本中的微量靶向代谢组学检测,有效助力研究团队获取了可靠的实验数据。
科似海生物长期致力于突破代谢质谱检测的技术瓶颈,专注于提供定制化的代谢研究解决方案。公司开发了多项核心技术,涵盖超微量样本代谢物检测、稳定同位素代谢示踪以及全景覆盖的代谢组学与脂质组学常规分析,致力于为客户提供可靠、精准的科学数据。
作为一家专注于攻克技术难点的研发与检测服务企业,科似海生物在组织、胚胎、细胞、培养基等微量及珍贵样本的小分子代谢组学和脂质组学检测方面积累了丰富经验,致力于为更多科研团队提供精准、可靠的技术服务,让“难检测、测不准”的微量样本,不再成为科研路上的障碍。如果您也面临微量/珍贵样本的代谢检测难题,欢迎联系科似海——我们期待成为您科研路上的“技术队友”,共同推动更多科学发现!