脂肪从头合成(DNL)是哺乳动物中生成脂质的重要过程,主要发生在脂肪组织和肝脏中。肝脏DNL的异常升高与胰岛素抵抗和代谢功能障碍相关脂肪性肝病(MASLD)密切相关。研究人员通过抑制DNL关键酶(如乙酰辅酶A羧化酶ACC和脂肪酸合酶FAS)来降低肝脏DNL,但完全抑制这些酶可能产生副作用。寻找新的靶点会对维持肝脏DNL稳态提供可行性的干预方案。细胞质乙酰辅酶A(AcCoA)是DNL途径的共同前体,靶向供应胞质AcCoA的特定线粒体或胞质途径,可能是一种在治疗上可行的替代方法,以取代在 ACC或FAS处抑制DNL的策略。多条通路可合成AcCoA,丙酮酸可以通过线粒体丙酮酸载体和柠檬酸载体轴(MPC-CiC轴)提供胞质AcCoA,胞质中的乙酸也可以通过乙酰辅酶A合成酶2(ACSS2)直接与辅酶A结合生成乙酰辅酶A。但是,关于这些途径的酶和底物如何在代谢上相互作用,以控制胞质乙酰辅酶A的可用性并促进肝脏DNL仍不清楚。
美国爱荷华大学卡佛医学院Eric B. Taylor团队研究发现丙酮酸和乙酸盐是肝脏DNL的主要底物,分别通过MPC-CiC轴和细胞质酶乙酰辅酶A合成酶2(ACSS2)介导。此外,酮体也可能通过乙酰乙酰辅酶A合成酶(AACS)为DNL提供底物。通过基因敲除小鼠模型和同位素追踪实验,揭示了MPC和ACLY在控制主要脂肪生成乙酰辅酶A产生途径中的关键作用,为选择性治疗调节策略提供了新的视角。相关研究成果2025年1月7日在线发表于Cell Metabolism杂志上。

研究结果
Part1:CiC LivKO小鼠减少由乳酸/丙酮酸供能的DNL,但不影响乙酸盐供能的DNL
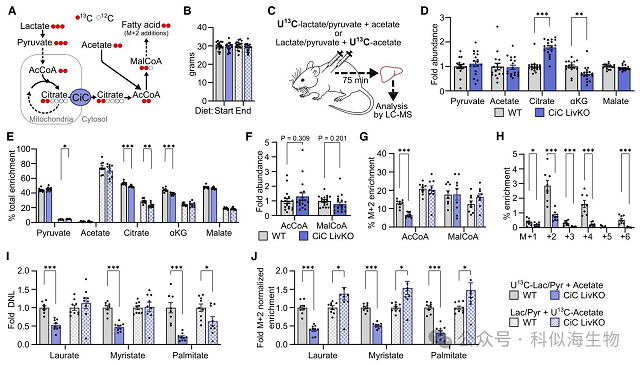
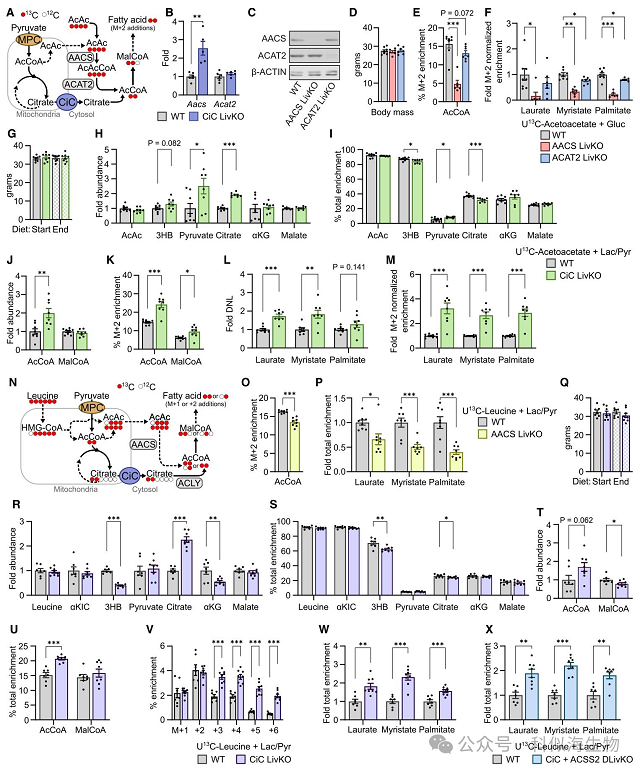
由于从2H2O 追踪重氢可以测量所有来源的DNL,但是,无法检测到底物利用的抵消变化。因此,研究团队使用13C标记来专门测试丙酮酸和乙酸盐作为DNL底物的使用情况。由于丙酮酸和乙酸盐具有不同的代谢命运和调节作用,他们设计了13C 标记交换的底物竞争测试,通过腹腔注射给予([U-13C]-乳酸/丙酮酸 [10:1以近似内源性氧化还原状态]+未标记的乙酸盐与未标记的乳酸/丙酮酸 [10:1]+[U-13C]-乙酸盐)。之后在特定时间提取肝脏极性和非极性代谢物,并通过靶向高分辨率液相色谱-质谱(LC-MS)分析13C富集情况。
通过对TCA循环代谢物丰度分析发现CiC LivKO肝脏中柠檬酸浓度增加,表明线粒体柠檬酸输出中断从而引起下游中间产物减少。为了研究CiC破坏对肝脏丙酮酸和乙酸盐供能的DNL的影响,他们测量了月桂酸(12:0)、肉豆蔻酸(14:0)和棕榈酸(16:0)脂肪酸中的13C富集。该分析表明,CiC LivKO减少了由丙酮酸供能的 DNL。令人惊讶的是,未观察到乙酸盐供能的DNL作为补偿的增加。
Part2:ACSS2 LivKO会减少由乙酸盐供能的DNL,但不会影响由乳酸/丙酮酸供能的DNL
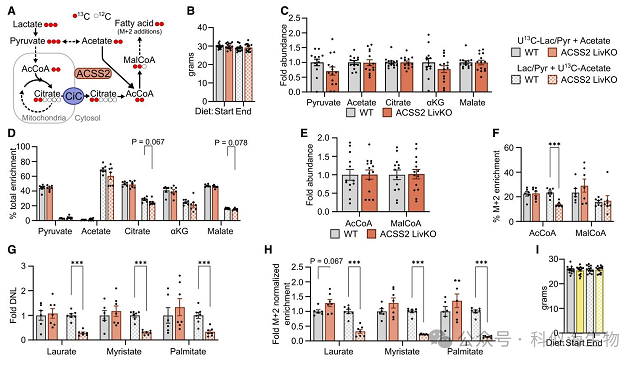
由于在CiC肝脏特异性敲除(CiC LivKO)小鼠中,由丙酮酸供能的DNL仍部分维持,他们进行了平行的13C标记底物竞争实验,以测试ACSS2在丙酮酸和乙酸盐用于DNL过程中的作用。与CiC LivKO不同,ACSS2 LivKO对TCA循环中间产物的丰度和富集程度影响极小。然而,与ACSS2直接从乙酸盐生成乙酰辅酶A的作用一致,13C-乙酸盐在乙酰辅酶A中的富集几乎减半。同样,来自乙酸盐的总脂肪酸和M+2标准化脂肪酸的13C富集显著降低。相反,ACSS2肝脏特异性敲除(ACSS2 LivKO)不会改变13C-乳酸/丙酮酸在乙酰辅酶A、丙二酰辅酶A或脂肪酸中的富集程度,但会使 M+2 标准化脂肪酸富集程度有接近统计学意义的增加。这些数据表明,ACSS2 LivKO 会减少由乙酸盐供能的从头脂肪生成(DNL),但不会影响由丙酮酸供能的DNL,并且降低了乙酸盐在DNL乙酰辅酶A前体池中的比例贡献。
Part3:ACLY肝脏特异性敲除减少由乳酸/丙酮酸供能的 DNL
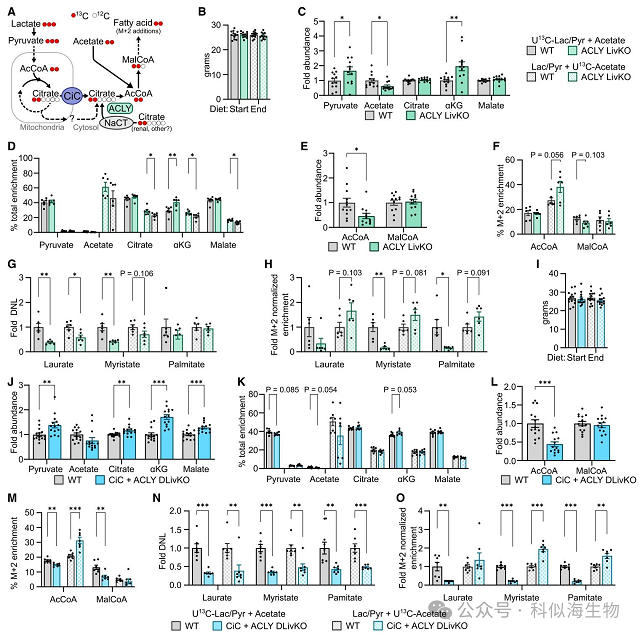
在排除了ACSS2介导的乙酸盐旁路作为维持CiC缺失后丙酮酸供能的DNL的途径后,他们将关注点放到不依赖CiC的细胞质柠檬酸来源。ACLY(ATP-柠檬酸裂解酶)可将线粒体输出的柠檬酸转化为乙酰辅酶A用于DNL,但也可以利用其他来源的柠檬酸。对野生型(WT)和ACLY肝脏特异性敲除(ACLY LivKO)小鼠按照上述方法进行平行的13C标记实验。结果表明,ACLY LivKO 增加了α-酮戊二酸(αKG)的丰度以及来自乳酸/丙酮酸的13C富集并使乙酰辅酶A丰度降低约一半。来自13C-乳酸/丙酮酸的乙酰辅酶A和丙二酰辅酶 A富集未发生变化,但来自13C-乙酸盐的乙酰辅酶A富集增加。值得注意的是,无论是总13C脂肪酸富集还是M+2标准化13C脂肪酸富集,ACLY LivKO与WT相比的缺陷似乎略大于CiC LivKO。这与CiC是细胞质柠檬酸的主要但并非唯一来源的观点一致。
由于CiC LivKO和ACLY LivKO的代谢效应明显不同,并且存在不依赖CiC从丙酮酸生成细胞质柠檬酸的途径的可能性,他们考虑联合敲除是否会累加降低DNL。为了验证这一可能性,他们构建了CiC+ACLY双基因肝脏特异性敲除(CiC+ACLY DLivKO)小鼠,并进行平行的13C标记交换实验。结果发现TCA循环中间产物的丰度,包括柠檬酸和αKG,均有所增加,但13C富集未发生变化,仅在提供13C-乳酸/丙酮酸时αKG富集略有增加。因此,CiC和ACLY双基因敲除的综合效应重现了单个CiC和ACLY LivKO中分别出现的柠檬酸和αKG水平的增加。总之,这些结果表明,CiC和ACLY发挥着不同的代谢作用,ACLY在控制细胞总乙酰辅酶A方面对CiC具有代谢上位性作用,并且CiC和ACLY协同控制由丙酮酸供能的DNL。
Part4:MPC 肝脏特异性敲除减少由乳酸/丙酮酸和乙酸盐供能的DNL
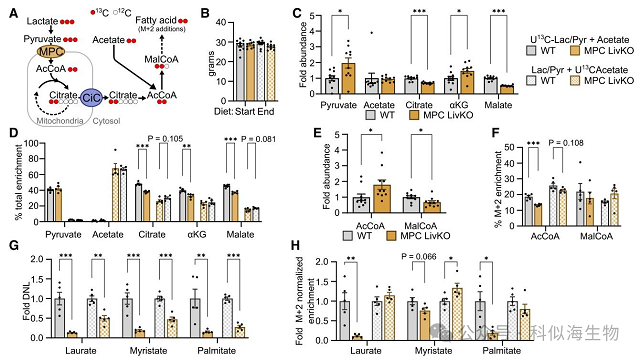
鉴于ACLY肝脏特异性敲除(ACLY LivKO)和CiC肝脏特异性敲除(CiC LivKO)在影响丙酮酸供能的DNL方面具有相似作用,接下来他们探究了通过线粒体丙酮酸载体(MPC)进行的线粒体丙酮酸转运作为二者上游步骤的调控作用。正如预期的那样,随着MPC功能的破坏,乳酸和丙酮酸的丰度增加,除αKG外的TCA循环中间产物减少。来自13C-乳酸/丙酮酸的TCA循环富集也减少,而对来自13C-乙酸盐的富集影响极小甚至没有影响,这与丙酮酸转运的特定缺陷相符。与CiC LivKO类似,MPC LivKO增加了乙酰辅酶A的丰度,降低了丙二酰辅酶 A 的丰度,同时伴随着来自乳酸/丙酮酸的乙酰辅酶A标记减少。MPC LivKO还降低了来自标记乳酸/丙酮酸的总13C脂肪酸富集,其影响明显大于CiC或ACLY缺失的情况。标记乳酸/丙酮酸的M+2标准化脂肪酸富集降低也证实了这一观察结果。这些结果共同表明,MPC 的缺失显著减少了丙酮酸通过CiC和ACLY进入 DNL以及DNL前体乙酰辅酶A池的通量。
与CiC LivKO和ACLY LivKO 不同,MPC LivKO 还显著降低了由乙酸盐供能的 DNL。然而,乙酸盐的M+2标准化脂肪酸13C富集变化极小。这些结果表明,尽管由DNL产生的总乙酸盐减少,但乙酸盐在DNL前体乙酰辅酶A池中的供应比例并未改变,这可能是因为与丙酮酸供能的DNL减少相比,乙酸盐供能的DNL减少幅度较小。这些数据表明,MPC的破坏直接限制了由乳酸/丙酮酸生成DNL前体乙酰辅酶A,但对乙酸盐没有影响。
Part5:CiC 肝脏特异性敲除(LivKO)增加了乙酰乙酸和亮氨酸用于从头脂肪生成(DNL)的利用率
鉴于在整个研究过程中观察到的DNL底物供应存在冗余现象,且无法用丙酮酸或乙酸代谢来解释,一个悬而未决的问题是,还有哪些其他途径可以为DNL提供乙酰乙酰辅酶A。有文献研究表明,酮体在体内和体外灌注组织中都可以作为从头脂肪生成(DNL)的底物。基于早期的生化研究,推测酮体供能产生胞质乙酰辅酶A的途径是:通过酶AACS将乙酰乙酸在胞质中硫酯化生成乙酰乙酰辅酶 A,然后由乙酰辅酶A乙酰转移酶 2(ACAT2)将其裂解,生成两个乙酰辅酶A分子。有趣的是,禁食的CiC肝脏特异性敲除(LivKO)小鼠肝脏中Aacs的转录水平升高,而Acat2的转录水平没有变化,这与在缺乏 CiC 的情况下,源自乙酰乙酸的胞质乙酰辅酶 A 生成上调相一致。
为了验证AACS和ACAT2在体内介导乙酰乙酸供能的肝脏DNL这一假设,研究团队在喂食正常饲料(NCD)的 AACS和ACAT2肝脏特异性敲除小鼠中追踪了[U-13C]-乙酰乙酸。敲除这两个基因中的任何一个都不会影响小鼠的体重。由于这是一项初步的原理验证实验,为了引发生理性胰岛素反应以刺激DNL,研究团队同时给予葡萄糖。AACS 肝脏特异性敲除小鼠的乙酰辅酶A和脂肪酸中13C富集度显著降低。相反,ACAT2肝脏特异性敲除的影响很小,这表明可能存在尚未确定的将胞质乙酰乙酰辅酶A转化为乙酰辅酶A的机制,很可能是通过其他硫解酶的活性实现的。由于在极端生理状态下,肝脏会发生高水平的酮体生成与净柠檬酸合成,研究团队假设酮体供能的DNL可能是一种起源于线粒体、不依赖于CiC的DNL途径。研究团队将13C- 乙酰乙酸与乳酸/丙酮酸共同注射。13C-乙酰乙酸会生成13C-β-羟基丁酸并与之达到平衡,这证实了其参与了内源性酮体代谢。CiC 肝脏特异性敲除导致柠檬酸丰度增加,13C-乙酰乙酸衍生的柠檬酸富集度略有下降。乙酰辅酶A的丰度增加,而丙二酰辅酶A的丰度没有变化。与追踪13C-乳酸/丙酮酸或13C-乙酸的结果形成鲜明对比的是,CiC肝脏特异性敲除使乙酰乙酸的13C富集度在乙酰辅酶A和丙二酰辅酶A中几乎增加了一倍。13C富集度的增加延续到DNL过程中,M+2标准化的脂肪酸13C富集度增加了约3倍。因此,CiC 肝脏特异性敲除显著上调了乙酰乙酸进入DNL和前体乙酰辅酶A的通量。
然后,研究团队考虑了支链氨基酸亮氨酸为酮体供能的DNL的潜力。在肝脏中,α-酮异己酸在线粒体中进一步代谢为乙酰乙酸和乙酰辅酶A,当有足够的回补底物时,后者可用于进一步的酮体生成或合成柠檬酸。重要的是,由于亮氨酸不能净生成线粒体草酰乙酸,它不是一种回补底物,因此不能为净柠檬酸合成提供原料。因此,亮氨酸是一种持续可用的、生理性的乙酰乙酸和线粒体乙酰辅酶A 来源,它可以通过AACS途径为DNL提供净原料,但只会标记而不会对线粒体输出的柠檬酸产生的脂肪酸做出净贡献。为了测试亮氨酸作为酮体供能的DNL前体的作用,研究团队首先在喂食正常饲料的AACS肝脏特异性敲除小鼠中追踪了[U-13C]-亮氨酸+乳酸/丙酮酸。亮氨酸很容易被用作DNL的底物,AACS肝脏特异性敲除显著降低了13C-亮氨酸在乙酰辅酶A和脂肪酸中的富集度。
在发现亮氨酸以 AACS 依赖的方式为肝脏 DNL提供原料后,他们测试了CiC肝脏特异性敲除对短期喂食高蔗糖饮食小鼠中亮氨酸来源的肝脏DNL的影响。与上述初步实验一样,将13C-亮氨酸与乳酸/丙酮酸共同注射并追踪其进入下游代谢产物。13C富集情况在很大程度上与追踪乙酰乙酸时的结果相似。CiC肝脏特异性敲除(LivKO)小鼠体内的柠檬酸增加,而aKG减少。重要的是,13C标记的亮氨酸和13C标记的aKG达到平衡,并使β-羟基丁酸的13C富集度超过60%,这表明亮氨酸脱氨生成α-酮异己酸的过程在介导强劲的亮氨酸驱动的酮生成中并非限速步骤。CiC LivKO 小鼠的β-羟基丁酸13C富集度和含量均降低,这可能是由于线粒体乙酰乙酸输出适应性增加所致。
由于[U-13C] 亮氨酸代谢为线粒体乙酰乙酸、乙酰辅酶 A 和柠檬酸时,会产生 M+1和M+2 的胞质乙酰辅酶 A,[U-13C] 亮氨酸进入脂肪酸合成途径会生成含偶数和奇数个13C的物质。CiC LivKO小鼠中,亮氨酸的13C富集进入M+1和M+2 的乙酰辅酶A同位素体的量增加,同时乙酰辅酶A的含量也有近乎显著的增加。值得注意的是,CiC LivKO小鼠的总脂肪酸13C富集度增加了约2倍。因此,对于CiC LivKO 诱导的酮体供能的 DNL上调,ACSS2 并非必需。总体而言,这些结果表明,外源性提供的和亮氨酸生成的酮体以 AACS 依赖的方式为肝脏 DNL 提供原料,并且抑制线粒体柠檬酸转运可上调酮体供能的DNL。
Part6:线粒体-胞质从头脂肪生成(DNL)供应网络的结构
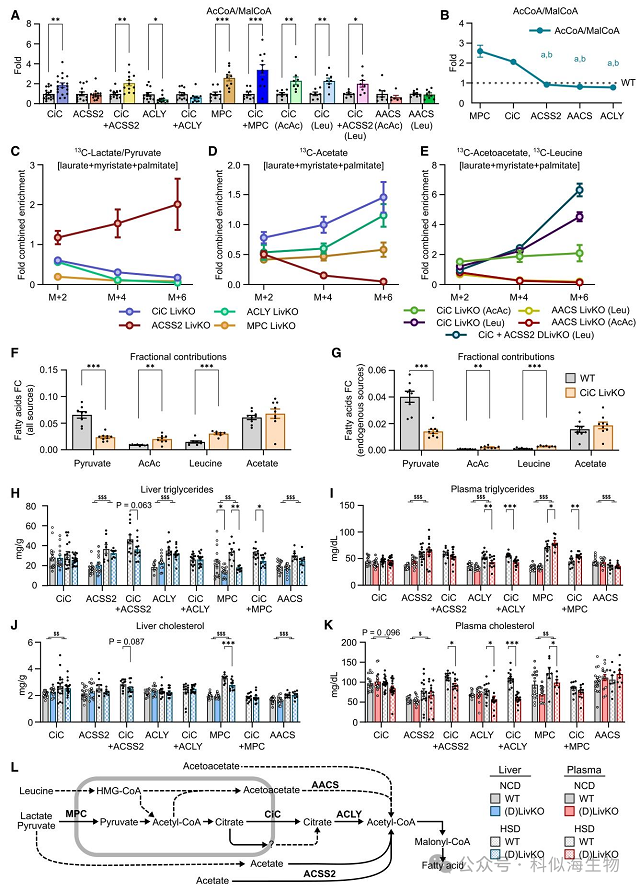
在这里,研究团队对多种基因模型采用相同底物混合物进行平行稳定同位素示踪,这提供了一个独特的对比机会。为了评估总乙酰辅酶 A 和丙二酰辅酶 A 库之间的关联,对于每一个13C示踪底物竞争实验,研究团队于每个样本计算乙酰辅酶 A/丙二酰辅酶A的丰度比。该比率描述了线粒体和细胞质中乙酰辅酶 A 库通过ACC反应生成丙二酰辅酶A的流量,而这是中心DNL途径的第一个必需反应。重要的是,这些丰度比考虑了所给予的乳酸/丙酮酸、乙酸、乙酰乙酸和亮氨酸以及内源性乙酰辅酶A的来源。这种动态状态下的全底物分析表明,CiC和MPC肝脏特异性敲除(LivKO)均会使乙酰辅酶 A /丙二酰辅酶 A 的比率升高,ASSC2 和AACS肝脏特异性敲除对此比率无影响,而 ACLY 肝脏特异性敲除会使其降低,即使与CiC基因敲除同时存在也是如此。引人注目的是,通过线秩图描绘不同基因型对乙酰辅酶 A/丙二酰辅酶 A 比率的相对主要影响,结果显示其范围超过 5 倍。这些分析呈现出一种清晰的模式,表明CiC和MPC肝脏特异性敲除(LivKO)会导致线粒体乙酰辅酶A积累,ACSS2和AACS对总乙酰辅酶 A 水平的影响极小,而ACLY是控制细胞质乙酰辅酶A水平的主要酶。这些数据共同证明了 MPC-ACLY 轴在调节乙酰辅酶A水平和区室化中的重要作用。
为了总结营养-基因相互作用对DNL的调控,研究团队通过总富集量和M+2标准化指标,比较了所有测试基因型中月桂酸+肉豆蔻酸+棕榈酸的13C富集情况。进一步通过绘制底物竞争实验中观察到的月桂酸+肉豆蔻酸+棕榈酸的折叠标准化同位素体丰度,对这些数据进行了浓缩,按乳酸/丙酮酸、乙酸、乙酰.中表现最为显著。这些数据表明,肝脏DNL底物供应网络有助于维持全身甘油三酯和胆固醇的稳态。总之,将本研究中评估的途径绘制在通路图中,可以展示线粒体-细胞质肝脏DNL底物供应网络的整体连通性和控制结构。
研究结论
MPC和ACLY调控主要的肝脏脂肪生成乙酰-CoA生产途径:线粒体丙酮酸载体(MPC)和ATP-柠檬酸裂解酶(ACLY)在肝脏脂肪生成中起着关键作用。
ACSS2依赖的DNL与MPC-CiC-ACLY途径并行:乙酰-CoA合成酶2(ACSS2)依赖的脂肪生成途径与MPC-CiC-ACLY途径并行运作。
AACS介导酮体生成乙酰-CoA和DNL:乙酰乙酰-CoA合成酶(AACS)在酮体生成乙酰-CoA和脂肪生成中起重要作用。
CiC缺失增加酮体生成乙酰-CoA和DNL:线粒体柠檬酸载体(CiC)的缺失会显著增加酮体生成乙酰-CoA和脂肪生成。
研究亮点
在本次研究中,科研团队巧妙运用了13C同位素示踪技术,精心设计并开展了底物交换竞争测试,旨在深入探究小鼠肝脏内脂肪从头合成途径的底物供应机制。同位素示踪技术宛如一把精准的 “代谢显微镜”,能够让被标记的底物在小鼠体内的代谢轨迹清晰地呈现于研究者眼前。凭借这一技术优势,科研人员得以精准量化代谢物在不同代谢通路中的贡献占比,为进一步揭开隐藏于其中的分子作用机制提供了强有力的研究支撑,有望为代谢相关疾病的研究与防治开辟新路径。
科似海生物同位素示踪技术服务
科似海生物提供专业且全方位的同位素代谢流检测服务。我们的技术资源丰富多样,提供涵盖13C、15N等在内的多种高品质示踪剂,以满足不同研究方向、不同层次的需求。无论是贴壁细胞、悬浮细胞,还是酵母、蓝藻、大肠杆菌,亦或是针对复杂的组织样本,我们都能依据其独特性质,量身定制专属的收样指南,并精心设计测定标记率实验流程,确保每一个样本都能得到精准、有效的检测。
在代谢通路的解析上,我们的检测范畴广泛且深入,全面覆盖了糖酵解、磷酸戊糖途径、核苷酸代谢、三羧酸循环(TCA 循环)、氨基酸代谢、脂肪酸合成、丙酸循环、一碳循环等诸多关键通路,如同在生命的微观代谢网络中精准 “布线”,不放过任何一个可能蕴含重大科研发现的节点。
不仅如此,科似海生物深知科研项目的多样性与特异性,因此可紧密围绕客户的检测目的,凭借深厚的专业积累与创新思维,量身定制个性化的标记实验方案,助力科研突破层层困境。
科似海生物已经与国内多家高校、科研院所及公司完成合作,累计服务 1000 + 客户群体,圆满完成 100000+ 样本的精细检测,用实力赢得口碑,持续为生命科学领域的蓬勃发展注入强大动力。