随着代谢研究范式从“单一组分的变化”向“系统网络重塑”跨越,一个核心科学命题亟待阐明:在细胞功能状态演进的关键节点,究竟是哪些核心代谢模块的流量重分配构成了驱动细胞命运决定的底层动力?
甲羟戊酸(Mevalonate,MVA)代谢通路处于生物合成与信号转导的交叉轴心,近年来其重要性在多种生命活动中被反复验证。该通路位不仅承担着胆固醇和甾体类分子的生物合成,更通过提供关键的前体物质,精细调控着蛋白质的异戊二烯化修饰(Prenylation)及多种下游信号转导。无论是在肿瘤细胞的恶性增殖调控,还是在机体代谢紊乱、营养干预或药物应激条件下,MVA 通路的通量重编程均表现出与表型变化高度同步。因此,依托系统、精准的代谢检测,已成为连接分子机制与功能表型的重要研究手段。
基于成熟的靶向代谢组学技术平台,科似海生物构建了甲羟戊酸代谢通路 LC-MS/MS 靶向定量检测服务,通过对关键代谢节点的系统覆盖,为科研人员提供可靠的数据支持。
一、甲羟戊酸代谢通路的生物学定位
从代谢网络的整体结构来看,甲羟戊酸代谢通路是一条高度保守、同时又具备强调控特性的基础代谢途径。该通路以乙酰辅酶A 为起点,经 HMG-CoA 合成酶和 HMG-CoA 还原酶等关键限速酶催化,生成甲羟戊酸,随后逐步转化为异戊烯焦磷酸(IPP)和二甲基烯丙基焦磷酸(DMAPP),并进一步合成法尼基焦磷酸(FPP)、香叶基香叶基焦磷酸(GGPP)等重要中间体,随后参与胆固醇、甾体激素、脂溶性维生素以及多种异戊类化合物的合成(Figure1)。
值得注意的是,MVA 通路的生物学意义并不局限于“合成原料”。通路下游的异戊类中间体广泛参与蛋白质异戊烯化修饰,这一过程直接影响多种小 GTP 酶的定位和功能,从而调控细胞周期、信号转导以及细胞迁移等关键生物学过程。正因如此,MVA 通路更像是一个代谢与信号之间的接口模块。当细胞对膜结构、信号分子或增殖能力的需求发生变化时,该通路的代谢通量与中间体分布往往首先发生调整。因此,MVA 通路并非单一的合成路径,而是一个高度整合、精细调控的代谢网络。
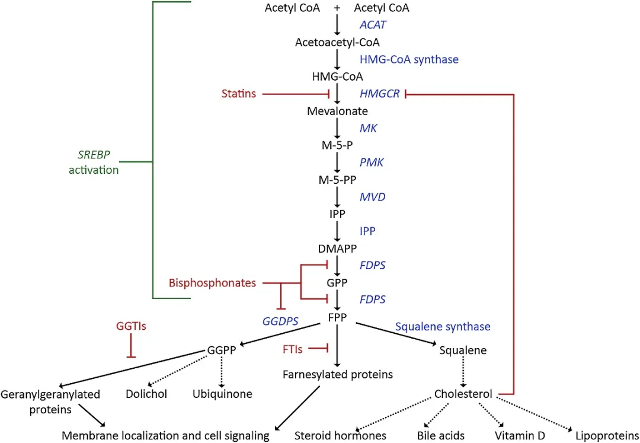
Figure. 1 MVA通路及其下游功能示意 [1]
在生理状态下,MVA 通路的代谢通量与细胞增殖、分化和代谢需求保持动态平衡;而在肿瘤、代谢性疾病或药物干预条件下,这一平衡往往发生显著重塑。通过对通路关键代谢物的系统性检测,可以从代谢层面捕捉这些动态变化,为机制研究提供直接证据。
二、为什么要关注甲羟戊酸代谢通路?
在实际研究中,单一代谢物的升高或降低,往往难以判断其真正的生物学意义。而 MVA 通路由于其明确的代谢顺序和功能指向,为通路解析提供了理想模型。
一方面,该通路处于多个重要生物合成路径的上游,其代谢状态的变化具有明显的“牵一发动全身”效应;另一方面,MVA 通路中多个节点受到严格酶学调控,其代谢物水平变化能够真实反映通路活性,而非随机波动。
近年来的研究不断表明,在疾病发生、药物干预或环境变化条件下,MVA 通路往往并非被动响应,而是作为主动重塑的代谢模块参与调控过程。基于靶向代谢组学的方法研究表明,对甲羟戊酸代谢通路中多个关键中间体进行并行定量,有助于从代谢层面评估通路整体活性变化[2]。因此,系统性地检测甲羟戊酸及其上下游关键代谢物,是从代谢层面定量解析通路功能状态(如激活、抑制或通量重新分配)的关键,可为后续的机制研究提供可靠的量化支撑。
三、甲羟戊酸代谢通路检测的主要应用场景
1.肿瘤代谢与靶向治疗研究
在肿瘤研究中,甲羟戊酸(MVA)代谢通路被认为是支撑肿瘤细胞快速增殖及逆境适应的关键代谢基础之一。以胰腺导管腺癌(PDAC)为例,Duttenhefner 等人在 2025 年发表的研究中,通过整合代谢组学与功能实验发现,PDAC 模型中 MVA 通路关键中间体(包括 FPP、GGPP 等)的水平显著升高,并与肿瘤细胞的侵袭能力和生存优势呈正相关[1]。进一步的通路干预实验表明,抑制该通路可影响肿瘤细胞的代谢可塑性及其对治疗的响应特征。
上述研究提示,MVA 通路并非仅作为胆固醇合成途径存在,而是在肿瘤细胞中被重塑为支持生长、存活及信号调控的重要代谢模块。在这一背景下,对通路关键代谢物进行靶向定量检测,有助于从代谢层面评估肿瘤细胞对 MVA 通路的依赖程度,并为代谢干预策略的机制研究提供数据支持。
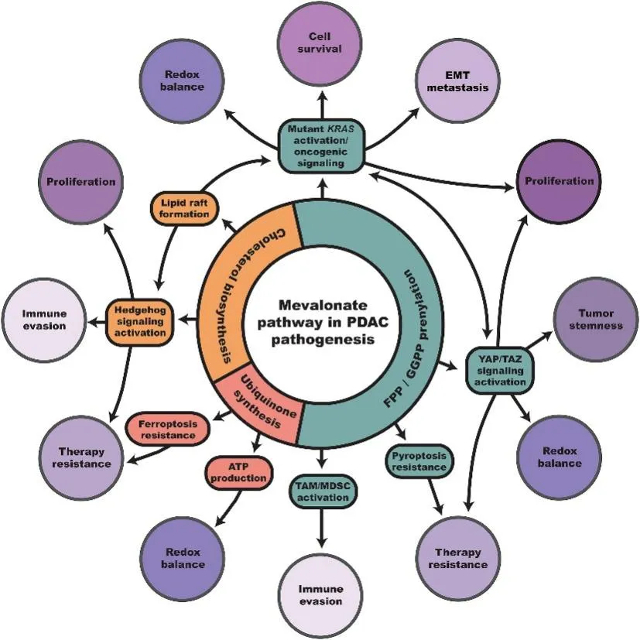
Figure. 2 MVA途径在胰腺导管腺癌中的致癌、免疫抑制和促生存作用[1]
2.代谢性疾病与遗传代谢异常研究
在代谢性疾病与遗传代谢异常的研究中,甲羟戊酸(MVA)通路的失调已被证实与疾病发生密切相关,具有关键的生物学意义。以 27-羟基胆固醇(27OHC)对肝细胞的影响为例,研究发现27OHC处理显著抑制了 MVA 通路相关酶的表达,并降低了胆固醇合成与糖酵解途径活性,这一代谢重塑过程揭示了MVA通路在脂质与能量代谢失衡中的关键调控作用[3]。基于靶向代谢组学对MVA通路关键代谢物的定量分析,可帮助揭示该通路在代谢异常背景下的动态调整,为疾病分型与机制解析提供实证数据支持。
3.生殖衰老与干预策略研究
最新研究揭示,MVA通路在女性生殖衰老及相关治疗方案中扮演了关键角色,为解析卵母细胞质量调控机制提供了全新视角。近期一项发表于 2025 年的研究通过靶向代谢组学与功能实验发现,MVA 通路下游代谢物法尼基焦磷酸(FPP)和香叶基香叶基焦磷酸(GGPP)通过增强小GTP酶的异戊烯化修饰显著改善老化卵母细胞的质量,这提示 MVA 通路中间体丰度变化与细胞功能状态密切相关[4]。因此,系统性监测这些关键中间体的动态变化,有望为代谢调节措施对细胞功能的影响提供代谢指标,并为揭示生殖衰老的代谢基础开辟新的研究路径。
四、技术优势
全覆盖的MVA代谢通路靶点检测
科似海围绕甲羟戊酸代谢通路进行系统化靶标布局,覆盖全通路代谢物及关键中间体,包括MVA、FPP、GGPP、IPP等,实现通路层面的全面解析,不遗漏核心信息。
高灵敏 LC-MS/MS 定量平台
依托精准成熟的 LC-MS/MS 靶向代谢质谱平台,采用优化后的液相色谱分离技术,搭配专属质谱检测参数,检测下限低至 fmol级别,同时兼顾该通路中低丰度中间代谢物的检测灵敏度与高丰度代谢物的定量稳定性,精准定量全通路代谢物浓度。适配各类细胞系、组织等常规量检测或微量类细胞、单细胞胚胎、脑脊液等珍贵微量样本类型。
通路针对性的前处理提取
结合MVA 通路代谢物理化特性,提供专属样本上机前处理试剂和标准化前处理流程以及内标质控校准体系。对MVA等水溶性代谢物和胆固醇等脂溶性代谢物分离提取,有效优化代谢物检测信号,确保样本从采集到检测的稳定性,最大限度保留样本真实代谢状态。
五、科似海生物甲羟戊酸通路检测列表
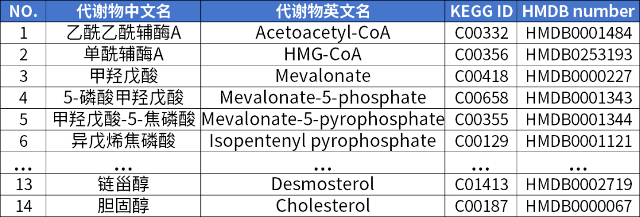
▼参考文献:
[1] Duttenhefner JN, Reindl KM. Mevalonate pathway in pancreatic ductal adenocarcinoma: mechanisms driving metabolic and cellular plasticity[J]. Cancer Pathogenesis and Therapy, 2026, 4: 110–123.
[2] Li J, Ju M, Zheng D, Wan H, Sun Y, Zhao J, Zhou L, Yin Q, Kang W, Song Y, Xue S. Simultaneous analysis of 7 key mevalonate pathway intermediates using liquid chromatography-orbitrap mass spectrometry. Analytical Biochemistry, 2025, 701: 115816.
[3] Shim WS, Lee S, Azamov B, Lee C, Kang Y, Lee KM, Hong C, Kwon SM, Kim K, Yoon JH, Song P. Proteomic analysis reveals inhibition of mevalonate and glycolysis pathways in hepatocytes by 27-hydroxycholesterol. Biochemical Journal, 2025, 482: 1011–1028.
[4] Liu C, Zhang H, Mao J, et al. Mevalonate metabolites boost aged oocyte quality through prenylation of small GTPases. Nature Aging, 2025, 5: 2022–2038.
科似海生物检测服务
科似海生物长期致力于突破代谢质谱检测的技术瓶颈,专注于提供定制化的代谢研究解决方案。公司开发了多项核心技术,涵盖超微量样本代谢物检测、稳定同位素代谢示踪以及全景覆盖的代谢组学与脂质组学常规分析,致力于为客户提供可靠、精准的科学数据。
作为一家专注于攻克技术难点的研发与检测服务企业,科似海生物在组织、胚胎、细胞、培养基等微量及珍贵样本的小分子代谢组学和脂质组学检测方面积累了丰富经验,致力于为更多科研团队提供精准、可靠的技术服务,让“难检测、测不准”的微量样本,不再成为科研路上的障碍。如果您也面临微量/珍贵样本的代谢检测难题,欢迎联系科似海——我们期待成为您科研路上的“技术队友”,共同推动更多科学发现!