代谢组学通过分析生物样本中的代谢物水平变化,为我们提供了了解生物体代谢状况的研究手段。这种静态代谢丰度分析能够反映细胞或组织器官在特定时刻的代谢特征。然而,由于代谢网络的复杂性(比如某一代谢物多种合成和消耗途径可以影响其静态丰度),仅凭静态丰度数据往往不能准确评估代谢通路的活跃程度。代谢流示踪技术则通过追踪代谢物在通路中的流动,定量分析代谢速率和通量,从而更深入地揭示动态的代谢过程。这种技术能够有效补充代谢组学数据的不足,为我们提供更全面的代谢信息,有助于阐明代谢变化的生物学机制。
代谢流示踪简介
代谢流示踪是一项利用稳定同位素标记追踪代谢物在生物体内的动态变化过程的技术。通过“给代谢物贴上标签”,我们可以清晰地观测代谢物的流动路径、反应速率以及在不同代谢通路中的分布情况。这种动态追踪使我们能够深入了解细胞内复杂的代谢网络,揭示其在正常生理状态或疾病状态下的运行规律。代谢流示踪应用在基础科学研究、药物代谢等方面,为发现生理病理机制和精准医学提供了有力支撑。
如果将代谢组学比喻为一张静态的照片,那么稳定同位素示踪代谢组学技术则是一段动态的视频。通过给代谢物‘挂上车牌’,即引入稳定同位素标记,我们可以追踪这些‘汽车’在代谢网络中的行驶轨迹,实时监测它们的流量变化和周转速率。这就好比在‘停车场’安装了无数个摄像头,不仅能记录下每个时刻的停车情况,还能追踪每辆车的行驶路线和停留时间。这种动态的追踪能力,使得我们能够更深入地理解细胞内代谢网络的运行规律,揭示其对环境变化、疾病发生等过程的响应机制[1]。
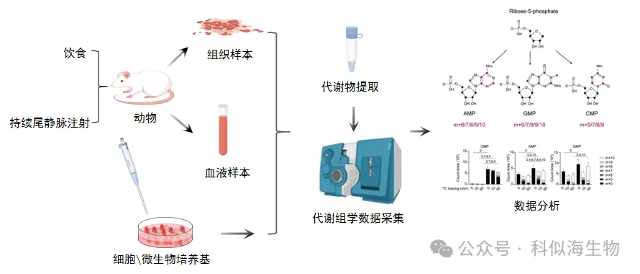
代谢流示踪技术在生命科学研究中具有广泛的应用前景。例如,在药物代谢研究中,我们可以通过追踪药物分子的代谢过程,了解药物的代谢途径、代谢产物以及药物-药物相互作用。在微生物代谢工程中,我们可以优化微生物的代谢途径,提高目标产物的产量。此外,代谢流示踪技术还可用于食品安全检测、环境污染物降解等领域。
代谢流示踪的方法
稳定同位素代谢流示踪是一种通过标记代谢物前体,以核磁、质谱等技术追踪代谢物在生物体内的流动途径,从而揭示代谢网络动态变化的技术。稳定同位素示踪实验有很多优势,但是在实施过程需要关注以下几个方面:
(1) 稳定同位素选择
稳定同位素的选择是代谢示踪实验的核心。最常用的同位素包括碳-13(13C)、氮-15(15N)、氧-18(18O)和氘(2H)等的。其中,全标记的示踪剂,如全13C标记的葡萄糖,可以同时标记多个下游代谢物,适用于大规模代谢通路分析。而特定位置标记的稳定同位素示踪剂,例如[1-13C]-glucose 和[1,2-13C]-glucose,可用于研究特定代谢途径,如磷酸戊糖途径[2]。又如3个13C标记的果糖[1,2,3-13C or 4,5,6-13C]-fructose 示踪剂可以用于研究小鼠小肠分解有机酸的过程[3]。由于含稳定同位素的示踪剂往往价格偏高,在开展同位素示踪实验时,需根据实验目的和预算进行综合考量,选择合适的示踪剂。
(2)递送方法
在细胞培养过程中,用含有稳定同位素标记的特定营养物质或化合物的培养基来培养细胞,使细胞在代谢过程中摄取并利用这些标记物,将稳定同位素整合到细胞的生物大分子(如蛋白质、核酸、脂质等)中,从而实现对细胞系的稳定同位素标记。对于动物实验,稳定同位素示踪剂的递送可以通过多种方式进行,包括饮食或管饲、静脉输注、腹膜注射等。
饮食或管饲
是一种较为自然的递送方式,但需要严格控制示踪剂在饮食中的含量和均匀性。
静脉输注
是当前应用最广泛的方法,它能够在规定的时间内以恒定速率将示踪剂注入血液,从而便于评估示踪剂在下游组织中的代谢产物情况。可有效减少因养分浓度瞬时大幅波动所引起的剧烈瞬态效应,从而提高实验结果的可靠性。然而,静脉输注具有一定的侵袭性,技术要求较高,实施成本也相对较高。
腹膜注射
是将药物或示踪剂直接注入动物腹腔的一种方法。腹腔内有丰富的血管和淋巴管,能够快速吸收注射物质并进入血液循环。
(3)标记时间递送方法
合适的同位素标记时间对实验的准确性、重复性和可靠性至关重要。不当的标记时间可能导致假阳性或假阴性结果。如果标记时间过短,会导致信号强度不足,遗漏重要的实验信息,引起假阴性结果。而过长的标记时间则可能因代谢物的再循环或降解而产生非特异性标记,还可能引发细胞生理状态的改变,进而出现一系列次生效应,影响正常生理和实验结果,产生假阳性结果。
以在细胞培养实验中的HeLa细胞(人宫颈癌细胞)为例,代谢标记达到稳态的时间因代谢途径的不同而有所差异[4-6]:
①糖酵解:约10分钟即可实现稳态标记(即“同位素稳态”)。为了捕捉糖酵解标记的动态过程,需要进行非常迅速的采样(例如,10秒的时间尺度)。
②三羧酸循环:约2小时可实现稳态标记。其动态过程可通过在15、30、60和120分钟等时间点进行采样来探测。
③核苷酸代谢:由于核苷酸合成和周转较慢,通常需要约24小时才能实现稳态标记。
在不知道标记达到稳态所需的时间的情况下,通常需要设计梯度时间来监测同位素化合物的标记情况,进而根据实验目的选择一个或多个标记时间进行多组平行实验,以确保实验的准确性。
代谢流示踪的应用领域
生物医学研究
代谢流示踪技术通过比较不同环境条件下不同代谢途径的流量分布变化,揭示疾病发生发展过程中的关键代谢通路的变化。这些信息有助于探究疾病机制、筛选诊断标志物,并为药物研发提供重要依据。
例如,在非小细胞肺癌研究中,向患者注入13C标记的乳酸后,发现 TCA 循环代谢物被广泛标记,这说明肿瘤细胞可以自主摄取乳酸并将其作为能量来源 。这一发现为开发靶向乳酸代谢抗肺癌药物提供了新的理论依据[3] [7]。
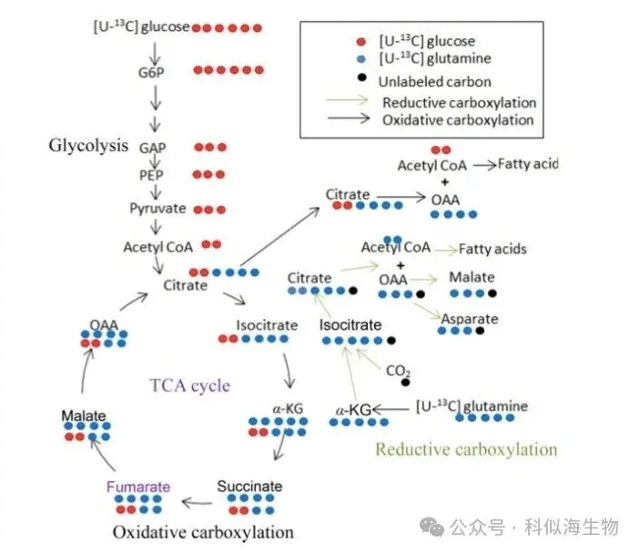
除此之外,代谢流示踪技术在药物研发与药效评估的研究中也发挥了至关重要的作用。例如,在乳腺癌研究中,研究人员使用 13C 标记的葡萄糖和谷氨酰胺发现,靶向代谢的药物能够显著抑制癌细胞的糖酵解和谷氨酰胺代谢,从而抑制肿瘤生长。这种技术为药物的筛选和优化提供了重要参考[8]。
同时,该技术也是研究疾病代谢状态异质性,干细胞分化和组织再生等领域的有力研究手段。例如,通过追踪13C标记的葡萄糖,研究人员发现干细胞在分化过程中从依赖糖酵解转变为依赖氧化磷酸化,这一代谢转变对干细胞的定向分化至关重要[9]。
合成生物学
代谢流示踪技术可以通过解析代谢网络,找到基因工程菌代谢网络中的关键节点和限速步骤,针对性的指导代谢途径改造和优化,最终有助于提高工程菌的产物产量、新型生物材料及解析复杂天然产物的合成机制研究。
①提高工程菌的产物产量
科研人员通过基因工程改造大肠杆菌生产生物燃料(如丙酮醇),利用 13C-代谢通量分析(13C-MFA) 追踪标记底物(如甘油)的碳流分布,精准解析代谢网络,助力科学家发现途径中的 “限速关卡”,针对性地优化基因表达、调整酶活性,大幅提升生物燃料的合成效率, 为生物燃料的高效合成与绿色能源开发提供了新思路。例如,在丙酮醇合成途径中,13C-MFA技术揭示 NADPH再生不足是限制产量的关键瓶颈[10]。通过过表达NADPH依赖的葡萄糖-6-磷酸脱氢酶(Zwf)或引入外源NADPH再生途径(如异柠檬酸脱氢酶Idh),显著提高了细胞内NADPH供应水平,最终使丙酮醇产量提升2.3倍[11]。
②新型生物材料及解析复杂天然产物的合成机制研究
对于新型生物材料的合成,同位素示踪代谢流同样是得力助手。在仿蜘蛛丝蛋白的研发中,研究团队利用15N 标记的氨基酸导入微生物培养体系,通过同位素示踪技术实时追踪标记氨基酸的聚合、折叠及纤维形成过程,从而优化仿蜘蛛丝蛋白合成的关键环节(培养条件和基因编辑策略等),使得人工合成的 “蜘蛛丝” 在强度、韧性等关键指标上不断逼近天然蛛丝[12] 。这种精准调控策略为生物基高性能材料(如医用缝合线、防弹纤维)的工业化生产奠定了基础。在解析复杂天然产物生物合成机制时,它更是不可或缺。以抗癌药物-紫杉醇 -为例,其合成涉及 植物-内生真菌共生体系中超过20步酶促反应。研究人员通过13C标记的紫杉烷前体(如紫杉二烯)追踪其在红豆杉细胞和内生真菌(如Taxomyces andreanae)中的代谢路径,发现共生真菌负责前体合成,而宿主细胞完成羟基化、酰化等关键修饰[13]。这不仅满足了科学家对自然奥秘的求知欲,更为人工半合成甚至全合成紫杉醇提供了理论蓝图,有望突破天然药物供应稀缺的瓶颈。
食品科学
稳定同位素示踪技术在食品及污染物溯源、食品掺假鉴别等方面显示出其独特的优势,为食品安全体系的完善提供可靠的理论依据,为食品全产业链的质量控制与监管提供了强有力的科学工具,助力实现“从农田到餐桌”的透明化管理。

①食品加工过程监控
以食品发酵为例, 科研人员利用13C标记糖类底物追踪酸奶发酵中乳酸菌的代谢过程。基于追踪标记物的代谢信息,生产者能微调发酵条件,提升酸奶口感与品质稳定性。此同位素标记技术满足了消费者对高品质酸奶的需求,展现了其在食品发酵领域的独特应用价值。
②食品营养代谢研究
以膳食纤维研究为例,研究人员将氘标记的膳食纤维加入到试验餐中,追踪其在胃肠道内的代谢路径,观察膳食纤维的分解、吸收及排泄情况。这些信息有助于食品研发人员设计更合理、更易于消化吸收的功能性食品,推动健康饮食潮流。
③食品安全检测
同位素技术可精准识别并溯源食品中污染物(如重金属、农药)。例如:通过铅同位素比值(206Pb/ 207Pb)可区分工业排放与自然背景铅污染,锁定大米、蔬菜中的铅污染源[14];利用15N标记的硝酸盐,可追踪化肥滥用导致的蔬菜硝酸盐超标路径。
④食品产地溯源与真实性鉴别
不同地理环境中土壤、水源及气候条件的同位素特征会通过食物链传递至农产品中,形成独特的“同位素指纹”。如,13C同位素作为蜂蜜的指示元素可以较好的判定蜂蜜是否存在掺杂[15]。同位素也在茶叶、乳制品、水产品、果蔬等溯源方面发挥着重要作用。
科似海代谢流示踪检测服务
科似海代谢流示踪检测服务始终秉持科学严谨的态度,自实验规划伊始,便扎根于深厚扎实的理论根基之上,全力确保每一项实验方案既具科学性,又兼顾合理性,为精准研究铺就稳固基石。而在至关重要的实验结果剖析环节,专业团队更是不遗余力,凭借精湛的技术与丰富的知识储备,展开深入细致的解析,并给予全面系统的评估,让每一个数据都能发挥最大价值。
在极具挑战性的小鼠同位素示踪实验领域,科似海生物凭借多年潜心钻研与实践积累,熟练驾驭持续尾静脉同位素示踪剂注射这一关键技术。该方法不仅能巧妙避开诸多潜在风险,切实保障实验动物的健康与安全,还大幅提升了标记的成功率,为您的科研探索之路注入强劲动力,一路保驾护航,助力您勇攀科研高峰。
亲爱的科研伙伴们,我们提供精准的检测服务,保证您实验数据的准确性和可靠性。我们坚信,通过我们的专业技能和优质服务,能够为您的科研工作提供强有力的支持。
此外,如果您在同位素示踪实验中遇到任何疑问,或有相关实验需要,请在文末留言或者添加科研客户微信,科似海生物将不遗余力地为您提供专业的咨询服务,解答您在实验过程中可能遇到的各种难题。
【参考文献】
[1] Linghu T, Tian JS, Qin XM, et al. Applications progress of stable isotopic tracer technique in metabolic regulation of endogenous substances[J]. Chin Tradit Herb Drugs (中草药), 2018, 49: 2678-2685.
[2] JyotiP, Shree M, Joshi C, Prakash T, Ray SK, Satapathy SS, MasakapalliSK.The Entner Doudoroff and Non oxidative Pentose Phosphate Pathways Bypass Glycolysis and the Oxidative Pentose Phosphate Pathway in Ralstonia solanacearum. mSystems. (2020) Mar 10;5(2):e00091-20.
[3] Jang C, Hui S, Lu W, Cowan AJ, Morscher RJ, Lee G, Liu W, Tesz GJ, Birnbaum MJ, Rabinowitz JD. The Small Intestine Converts Dietary Fructose into Glucose and Organic Acids. Cell Metab.(2018) Feb 6;27(2):351-361.e3.
[4] DeBerardinis, R. J., et al. (2007). The biology of cancer: metabolic reprogramming fuels cell growth and proliferation. Cell Metabolism, 7(1), 11-20.
[5] Zamboni, N., et al. (2009). 13C-based metabolic flux analysis. Nature Protocols, 4(6), 878-892.
[6] Lane, A. N., & Fan, T. W.-M. (2015). Regulation of mammalian nucleotide metabolism and biosynthesis. Nucleic Acids Research, 43(4), 2466-2485.
[7] Brandon Faubert et al. Lactate Metabolism in Human Lung Tumors. Cell. (2017) Oct 5;171(2):358-371.e9.
[8] Faubert, B., et al. (2020). Metabolic reprogramming and cancer progression. Science, 368(6487), eaaw5473.
[9] Zhang, J., et al. (2018). "Metabolic regulation of cell fate and function." Nature Reviews Molecular Cell Biology, 19(4), 213-228.
[10] Chen, X., et al. (2021). "Deciphering NADPH limitation in microbial cell factories using 13C-MFA." Metabolic Engineering, 67, 220-231.
[11] Zhang, Y., et al. (2022). "Enhancing NADPH supply for improved bioproduction in engineered E. coli." Biotechnology and Bioengineering, 119(5), 1320-1335.
[12] Rising, A., et al. (2021). "Spider silk proteins: Recent advances in recombinant production, structure-function relationships, and biomedical applications." Advanced Materials, 33(28), 2006495.
[13] Zhou, Y., et al. (2020). "Deciphering the taxol biosynthesis pathway in plant-fungal symbiosis." Nature Communications, 11(1), 1-12.
[14] Bi, X., et al. (2021). "Lead isotope ratios for tracing heavy metal contamination in rice." Environmental Science & Technology, 55(8), 4981-4989.
[15] Schellenberg, A., et al. (2020). "Detection of honey adulteration by stable isotope analysis." Journal of Agricultural and Food Chemistry, 68(3), 805-812.