PART-01
代谢组学:解码生命的化学密码
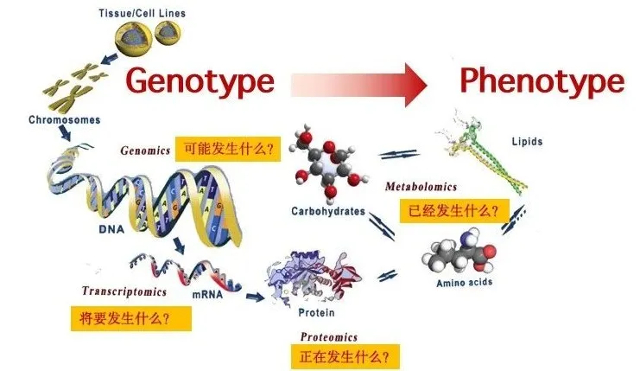
代谢是生物体内所有生化反应的集合体系,构成了生命体维持稳态的物质与能量基础,同时也是解析生命活动规律的核心研究对象。作为连接基因型与表型的关键桥梁,代谢网络直接反映了生物体的生理状态和功能特征。
代谢物(metabolites)身为生物学进程的 “收官之作”,它们呈现出的每一丝状态波动,都如同精准的晴雨表,忠实地映射出细胞功能的细微变化。当下,诸多棘手病症,像是令人闻风丧胆的癌症、隐匿难缠的肝病、迁延难愈的肾病、凶险突发的心血管病,以及错综复杂的神经性疾病等,无一不与细胞内代谢状态的失衡紊乱紧密相连。也正因如此,代谢组学在前沿科研领域强势崛起,一跃成为后基因组学时代不可或缺的锐利工具。代谢组学(metabolomics)巧妙融合高通量分析技术与生物信息学方法,借助前沿的检测手段,对代谢产物细致入微地进行种类甄别、数量测定以及变化规律追踪,仿若抽丝剥茧般,逐步揭开生命活动背后隐藏的本质机制,为疾病的早期预测驱散迷雾,为精准诊断指明方向,为科学分型提供依据,源源不断地挖掘出新的生物标志物,已然成为推动精准医学大步迈进的关键核心技术。
代谢组学依据研究目标的差异,可进一步细分为非靶向代谢组学与靶向代谢组学。本文通过对这两种研究策略的比较分析,期望能为科研人员在实验设计阶段提供具有针对性的方法学参考,助力精准选择适配的研究路径。并呼吁科研工作者不要一味的追求低价检测项目,希望能够在明确清晰了解检测项目背后的原理和缺陷之后,找到自己合适的检测方法进行应用。往往一步精准到位的检测能达到事半功倍的效果。
非靶向代谢组学
(Untargeted Metabolomics)
简介
非靶向代谢组学不预设目标代谢物旨在无偏向地检测生物样本中尽可能多的代谢物,采用 “撒网捕鱼” 的策略,为探索性研究提供代谢物信息,以发现潜在的生物标志物和代谢通路变化,适用于探索性研究领域。主要采用LC-MS、GC-MS、NMR等先进技术对细胞、组织、器官或生物体在受到刺激前后,小分子代谢物(主要是相对分子量1000 Da以内的内源性小分子化合物)的动态变化进行检测。
特点

应用场景
广泛应用于疾病机制研究、药物研发、环境毒理学等领域。例如,在疾病研究中,可用于发现疾病相关的新型生物标志物,了解疾病发生发展过程中的代谢变化规律;在药物研发中,可用于评估药物的疗效和毒性,探索药物作用的代谢靶点。非靶组学在食品安全,环境监测等领域也有广泛的应用。
技术方法&数据分析
非靶向代谢组学主要采用高分辨质谱技术triple TOF 或 QE 系列采集原始数据。运用XCMS、MZmine和MarkerView等工具对原始数据进行处理,采用主成分分析(PCA)、偏最小二乘判别分析(PLS-DA)、正交偏最小二乘判别分析(OPLS-DA)等常用分析方法结合t检验和变量权重重要性排序(VIP)值进行筛选差异代谢物。在代谢通路分析方面,利用HMDB、KEGG、Metlin、MetaCyc、mzCloud等常见的代谢组学通路数据库,进行代谢通路和互作网络的分析。
局限性
1.代谢物定性困难,假阳性率高
代谢物种类庞大繁杂,许多代谢物的化学结构相似,即使采用高分辨率质谱技术,也难以保证实现所有代谢物的精准无误的鉴定。此外,数据库的不完善也限制了代谢物的准确鉴定。由于缺乏标准品,非靶向代谢组学在检测过程中可能会产生许多假阳性信号,这增加了数据解释的难度,并可能影响研究结果的可靠性。
2.灵敏度较低,低丰度代谢物易被遗漏
尽管非靶向代谢组学具有高通量的优势,但其检测灵敏度仍然有限。对于低丰度的代谢物,非靶向代谢组学可能无法检测到其存在或变化。这限制了其在研究低丰度代谢物相关生理病理机制中的应用。
3.数据量大,分析复杂且耗时
非靶向代谢组学能够检测到大量的代谢物,产生海量的数据。然而,这些数据的处理和分析需要高水平的专业知识和先进的生物信息学工具。数据处理过程复杂,包括数据预处理、代谢物鉴定、统计分析等步骤,每一步都可能影响结果的准确性。
注意事项
非靶代谢组学以其价格低廉,无偏向性检测的“优势”被众多探索初期的科研工作者所青睐。但是选择非靶向代谢组学技术时,还需注意两大核心问题:避免滥用与警惕低质数据。
非靶代谢组学在数据解析环节依赖自建数据库或公共数据库进行代谢物匹配,但由于各数据库收录范围、注释标准存在显著差异,且普遍存在物种特异性代谢物覆盖不足的问题,导致代谢物鉴定准确率低。同时,不同仪器型号在灵敏度、分辨率上的差异,会造成低丰度代谢物的漏检,特别是在复杂生物样本中,这种缺失率会显著上升引发低质量数据,导致后期验证中难以重复。上述问题不仅可能引发代谢通路误判,还会导致实验结果在重复验证时出现显著偏差,严重制约非靶向代谢组学的研究可靠性与结论普适性。
非靶代谢组学虽能无偏检测代谢物谱,但若样本量不足或已经有了明确的研究范围(如聚焦特定通路),此时如果盲目使用易致资源浪费与无效分析。
因此,在某些特定研究中,靶向代谢组学凭借其高覆盖度与精准性优势,反而可能超越非靶代谢组学的应用价值。通过针对性设计检测面板,靶向技术可实现对目标代谢物的高灵敏度定量,在已知代谢网络或关键代谢物筛选场景中,其数据深度与可靠性常优于非靶策略。

靶向代谢组学
(Targeted Metabolomics)
简介
靶向代谢组学针对已知的代谢物或生物标志物进行定量分析,通过已知的标准品进行绝对定性定量分析,提高检测的灵敏度和准确性。采用“精准钓鱼” 的策略,为验证性研究提供准确可靠的数据支持,以便深入了解特定代谢物在生物过程中的作用。这种方法在特定代谢途径或疾病标志物的深入研究中具有独特优势。
特点

应用场景
在临床诊断、药物疗效监测、代谢调控机制研究等方面具有重要应用。比如,在临床诊断中,可用于对疾病生物标志物的定量检测,辅助疾病的诊断和病情评估;在药物疗效监测中,可通过监测药物作用靶点相关代谢物的变化,评估药物的治疗效果和患者的依从性。
技术方法&数据分析
靶向代谢组学常使用高灵敏度的质谱仪,如Sciex Qtrap 6500+等,结合多反应监测(MRM)或选择反应监测(SRM)模式,实现对目标代谢物的特异性检测和定量分析。
在靶向代谢组学方法中,天然和同位素标记的标准品的应用极大地促进了代谢产物的准确鉴定和定量,有效减少了假阳性结果的出现。定量代谢组学技术能够用于在组织或生物体中确立代谢物的基线水平,为实验组间的比较提供基准。此外,采用同位素标记的内标(IS)可以有效校正基质诱导的电离效应对分析精度的影响,进而提升生物反应检测试验的灵敏度。
靶向代谢组学由于关注的是特定种类的代谢物,因此其数据分析相较于非靶向代谢组学更为简洁明了。使用的方法和数据库针对特定的代谢物,因此在数据分析上提供了更为专业和针对性的结果。靶向代谢组学可将检测灵敏度提高至皮克级,能够捕捉到样本中极微量代谢物的变化。
局限性
靶向代谢组学针对预先设定的目标代谢物进行分析,可能会遗漏一些未知的信息;此外,对特定代谢物的精确定量分析需要经过多个繁琐的步骤,从样本的采集、处理,到标准品的选择、校准曲线的建立,再到数据的采集和分析,每一个环节都需要高度的精确性。这一系列复杂的操作使得整个分析过程耗时较长。
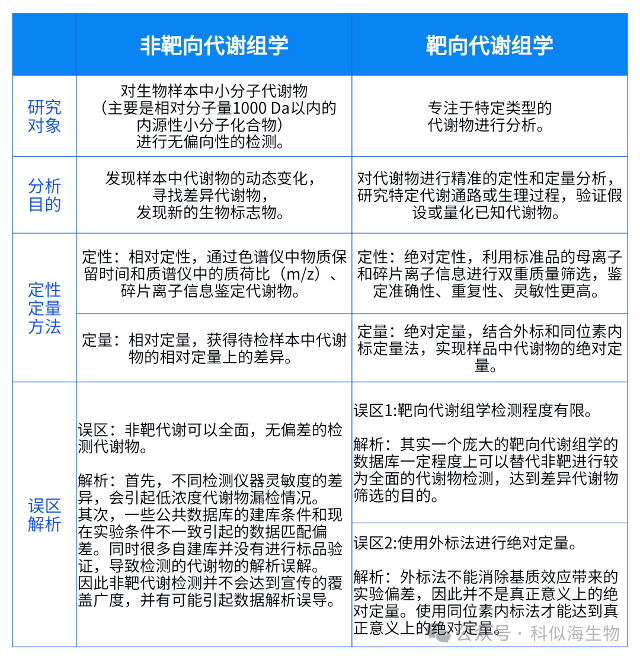
两者差异性的总结表
PART-02
如何选择靶向还是非靶向?
两种代谢组学在检测目标存在差异。非靶向代谢组学侧重于无偏向性的检测代谢物,而靶向代谢组学则专注于特定种类代谢物进行检测。由于两者所针对的目标代谢物有所不同,可以根据具体的检测对象,有针对性地选择检测方式,以便更快速地获得所需的检测结果,并提高检测数据的准确性。
场景一:实验目的不明确,想“撒网”探索代谢变化
推荐方案:非靶向代谢组学
当实验目的完全不明确时,可以选择非靶向代谢组学。非靶向代谢组学能够无偏向性的检测样本中的代谢物,有助于发现新的代谢物和代谢途径,为后续的深入研究提供线索。
适用情况:
疾病机制研究(如急性肝衰竭、糖尿病)中寻找潜在标志物。
环境暴露、药物干预或基因编辑后的全局代谢响应分析。
场景二:已知目标代谢物范围,需精准定量
推荐方案:灵活选择靶向或“非靶向+靶向”组合
当已知要检测的物质的大概范围,或者对特定代谢物有明确的研究兴趣时,可以根据情况选择靶向代谢组学或“非靶向+靶向”组合检测。靶向代谢组学能够针对特定的代谢物进行精确定量分析,提供准确、可靠的数据支持,有助于深入研究特定代谢物的功能和作用机制。非靶向和靶向代谢组学的结合应用,可以更加全面、深入地了解代谢物的变化和功能,为疾病的诊断和治疗提供有力的支持。
适用情况:
目标代谢物少且需高灵敏度(如临床诊断标志物):直接选择靶向代谢组学。例:糖尿病研究中检测血糖、胰岛素等10-20种标志物。
目标范围宽泛不确定研究方向:先通过非靶向组学进行筛选,再利用靶向代谢组学进行验证。例:通过非靶向组学结果发现肝癌患者胆汁酸异常后,再使用靶向组学定量20种胆汁酸亚型。
场景三:大队列样本的初期筛选
推荐方案:非靶向代谢组学为主
在进行大队列数据的初期筛选时,可以选择非靶向代谢组学。非靶向代谢组学能够快速、高通量检测样本中的代谢物,帮助研究人员筛选出潜在的差异代谢物,为后续的靶向代谢组学研究提供目标和方向。但是后期还是需要靶向进行进一步验证确保数据的可信度。
适用情况:
人群队列研究、流行病学调查。
大规模药物筛选或环境污染物暴露评估。

常见误区解答
Q:非靶向和靶向必须二选一吗?
A:非靶向用于“撒网”发现差异代谢物,靶向用于“精准”验证候选标志物,如何选择需基于研究的具体需求、目标、资源条件以及研究阶段来决定。在某些情况下,靶向代谢组学也能够满足差异代谢物的筛选,如果完全不了解研究方向时,可结合两种方法双管齐下,既能广泛探索代谢物谱,又能够验证特定代谢物的变化。因此,在实际研究中,应根据具体情况灵活选择或结合使用这两种方法。
Q:非靶代谢组如何选质谱平台?GC还是LC
A:代谢物分布广、性质差异大,单靠一种分离分析手段难以进行无偏向的全面分析,应根据样品的性质及研究目的来选择并综合利用多种技术平台。根据两个平台的灵敏度和偏好性,可以根据研究关注目的进行选择。对于挥发和半挥发性的物质,比如游离脂肪酸,VOA等物质可以选择GC-MS,而LC-MS使用的物质范围则相对更为广泛一些。
科似海生物
提供非靶向与靶向代谢组学“双引擎”服务
科似海生物作为代谢组学领域的专业服务引领者,为投身疾病生物标记物探索和分子机制探究的科研工作者,量身打造全方位且极具专业水准的一站式服务。
在非靶向代谢组学板块,我们依托高灵敏度的质谱前沿技术,通过先进的生信分析手段,从海量数据中严谨筛选有差异的代谢物,深入开展通路解析,并持续跟踪后续验证检测工作,确保数据的可靠性,助力科研工作者寻找疾病的生物标志物。这一“撒网捕鱼”的策略,为探索性研究提供了广阔的视野。
在靶向代谢组学方面,科似海生物充分发挥专业优势,聚焦于对前期已发掘的生物标志物展开深度验证工作,并致力于扩建靶向组学数据库,希望更好的应用于生物标志物发掘。同时精心推出定制化的靶向组学方法开发专属服务。借助Sciex Qtrap 6500+等高灵敏度质谱仪,对代谢物进行绝对定量,确保数据的准确性和可靠性。这一“精准钓鱼”的策略,为验证性研究提供了有力的支持。
科似海生物拥有专业的技术团队和定制化的服务方案,从方案设计到技术平台,再到数据分析,我们提供一站式服务,助力科研与临床。无论是探索性研究还是验证性研究,科似海生物都能以专业的技术和定制化的方案,解锁代谢研究的无限可能,为生命科学的发展贡献力量。
【参考文献】
[1] 范仕成,高悦,张慧贞,黄民,毕惠嫦.非靶向和靶向代谢组学在药物靶点发现中的应用[J].药学进展,2017,41(04):263-269.
[2] 赖博文,刘玢,梁永康.基于高分辨质谱的非靶向代谢组学在食品造假鉴定中的研究进展[J].生物技术通报,2019,35(02):192-197.
[3] Ribbenstedt A, Ziarrusta H, Benskin J P. Development, characterization and comparisons of targeted and non-targeted metabolomics methods[J]. PloS one, 2018, 13(11): e0207082.
[4] Yong Fan et al. Comprehensive Metabolomic Characterization of Coronary Artery Diseases. JOURNAL OF THE AMERICAN COLLEGE OF CARDIOLOGY. VOL. 68, NO. 12, 2016.
[5] Peng Zheng et al. Plasma Metabonomics as a Novel Diagnostic Approach for Major Depressive Disorder . J. Proteome Res. 1/27/2012.
[6] Alseekh S, Aharoni A, Brotman Y, et al. Mass spectrometry-based metabolomics: a guide for annotation, quantification and best reporting practices[J]. Nature methods, 2021, 18(7): 747-756.
[7] Sumner L W , Amberg A , Barrett D ,et al.Proposed minimum reporting standards for chemical analysis Chemical Analysis Working Group (CAWG) Metabolomics Standards Initiative (MSI)[J].other, 2007, 3(3).DOI:10.1007/s11306-007-0082-2.