嘌呤核苷酸是生命活动的基本分子单元,参与核酸合成、能量代谢与信号转导等多种关键过程。嘌呤代谢异常与痛风、免疫缺陷、神经退行性疾病及恶性肿瘤等多种疾病相关。硫嘌呤类药物是临床常用的抗代谢药物,可通过干扰嘌呤代谢发挥抗肿瘤与免疫抑制作用;其疗效与毒性存在显著的个体差异,因此亟需借助精准的代谢物分析手段以实现个体化治疗指导。近年来,基于液相色谱-串联质谱(LC-MS/MS)的靶向代谢组学与稳定同位素示踪技术能对嘌呤等核苷酸类代谢物实现高准确度、高灵敏度的定量分析及代谢过程动态追踪,二者的结合已成为解析代谢通路动态调控、探究药物作用机制的关键技术手段。本文将重点介绍靶向组学和同位素示踪技术在揭示嘌呤代谢调控机制及其与硫嘌呤药物敏感性关系方面的应用,并在整合相关实例进行阐述。
本文介绍的研究于2025年11月发表在《Science》的一篇标题为“NUDT5 regulates purine metabolism and thiopurine sensitivity by interacting with PPAT”的研究论文。该研究系统揭示了NUDT5在调控嘌呤代谢平衡及硫嘌呤类药物敏感性中的新机制,并提示NUDT5的表达水平或其与PPAT的相互作用状态可能作为硫嘌呤个体化用药的潜在生物标志物。

摘要
细胞通过从头合成(DNPB)与补救合成两条途径维持嘌呤核苷酸稳态。嘌呤积累可通过反馈抑制机制降低DNPB活性,从而避免能量浪费。DNPB过度激活与神经系统功能障碍及高尿酸血症等疾病相关,然而其与补救合成途径之间的协调调控机制尚未完全阐明。本研究通过全基因组CRISPR筛选及稳定同位素示踪分析发现,Nudix水解酶5(NUDT5)在嘌呤补救途径激活时可抑制DNPB。NUDT5缺失会导致细胞在天然嘌呤或硫嘌呤药物存在时仍持续进行DNPB,进而产生对硫嘌呤类药物的耐药性。值得注意的是,该调控作用并不依赖于NUDT5已知的ADP-核糖水解酶活性,而是通过其与DNPB限速酶——磷酸核糖焦磷酸酰胺转移酶(PPAT)的相互作用,促进嘌呤体(purinosome)解聚,从而抑制DNPB。破坏NUDT5与PPAT之间的相互作用即可导致DNPB持续激活,并诱导硫嘌呤耐药。综上所述,NUDT5是调控DNPB与补救合成之间平衡的关键因子,其通过非酶学机制影响嘌呤代谢及硫嘌呤药物疗效[1]。
研究结果
PART-01
NUDT5缺失导致硫嘌呤耐药且
不依赖于其催化活性
通过全基因组CRISPR筛选,本研究首次发现NUDT5是硫嘌呤药物毒性的正向调控因子。实验证实,NUDT5敲除细胞对6-硫代鸟嘌呤(6-TG)和6-巯基嘌呤(6-MP)表现出与HPRT1敲除类似的显著耐药性。功能回补实验进一步显示,催化失活突变体NUDT5ᴱ¹¹²Q能够完全恢复细胞对硫嘌呤的敏感性,同时该突变体的ADP-核糖水解活性确已丧失。这一结果表明,NUDT5在调控硫嘌呤敏感性中的作用不依赖于其经典的酶催化功能,提示其可能通过非催化机制参与嘌呤代谢调控。
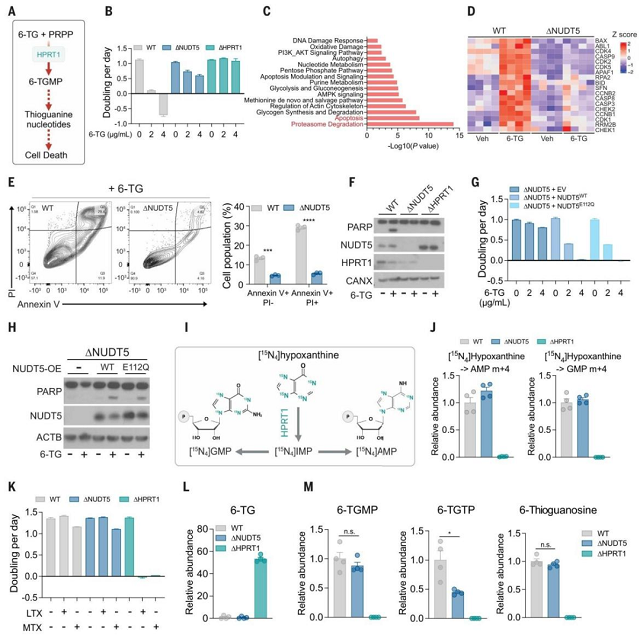
图1
PART-02
NUDT5抑制嘌呤
从头合成途径
为明确NUDT5是否影响嘌呤补救途径,研究采用¹⁵N₄次黄嘌呤进行同位素示踪分析。结果显示,NUDT5敲除细胞通过HPRT1将次黄嘌呤掺入AMP和GMP的效率与野生型细胞无显著差异。在6-TG处理后,NUDT5敲除细胞仍能正常生成6-TGMP、6-TGTP等毒性代谢产物,说明NUDT5并不直接影响嘌呤补救途径的代谢能力。代谢组学分析进一步发现,6-TG处理可显著降低野生型细胞中嘌呤核苷酸水平,并抑制线粒体氧化代谢,表现为氧化磷酸化减弱、氧耗率下降及谷氨酰胺还原性羧化作用增强。这些代谢变化在NUDT5敲除细胞中均被消除。以上结果证实,NUDT5是6-TG抑制嘌呤从头合成及相关代谢重塑所必需的调控因子。
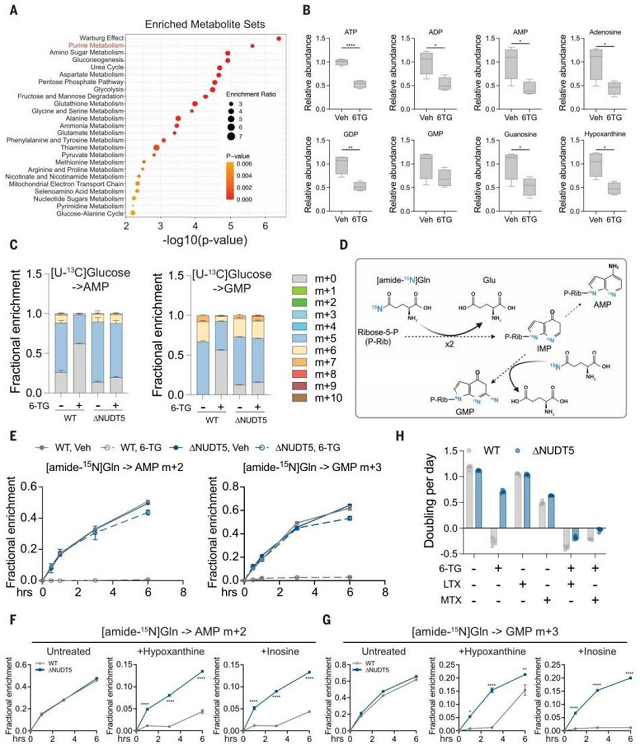
图2
PART-03
NUDT5与PPAT存在直接相互作用
并调控嘌呤体解聚
蛋白质互作网络分析与免疫共沉淀实验证实,NUDT5与PPAT之间存在直接相互作用。活细胞成像实验显示,在补充次黄嘌呤诱导嘌呤补救后,野生型细胞中的嘌呤体迅速完全解离;而在NUDT5敲除细胞或回补了互作缺陷突变体NUDT5ᴿ⁷⁰A的细胞中,嘌呤体解离过程显著延迟。同时,NUDT5缺失或表达R70A突变体也削弱了由次黄嘌呤或肌苷补充所引发的DNPB抑制。结构预测提示,NUDT5二聚体与PPAT四聚体可形成复合物,其中NUDT5的R70残基是互作界面的关键位点。因此,NUDT5通过结合PPAT促进嘌呤体解离,进而抑制DNPB。
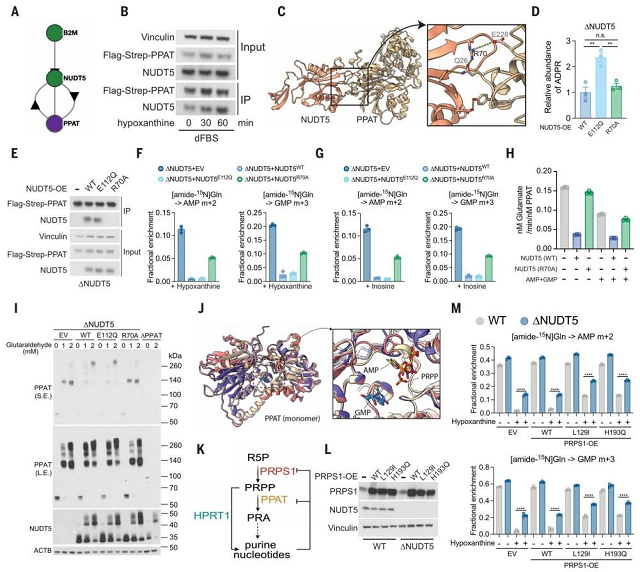
图3
PART-04
破坏NUDT5-PPAT互作
可导致硫嘌呤耐药
在硫嘌呤存在下,表达NUDT5ᴿ⁷⁰A的细胞与NUDT5敲除细胞一样,能够维持较高的DNPB活性,并表现出显著的生长优势和凋亡抵抗。这证明NUDT5与PPAT的物理结合主导了对DNPB的抑制和对硫嘌呤的敏感性,而非其酶活。NUDT5敲除并未减少6-TG诱导的DNA损伤,且细胞对其他DNA损伤剂也无交叉耐药性,表明其作用并非通过增强泛DNA损伤修复实现,而是特异性地调控嘌呤代谢以应对硫嘌呤压力。
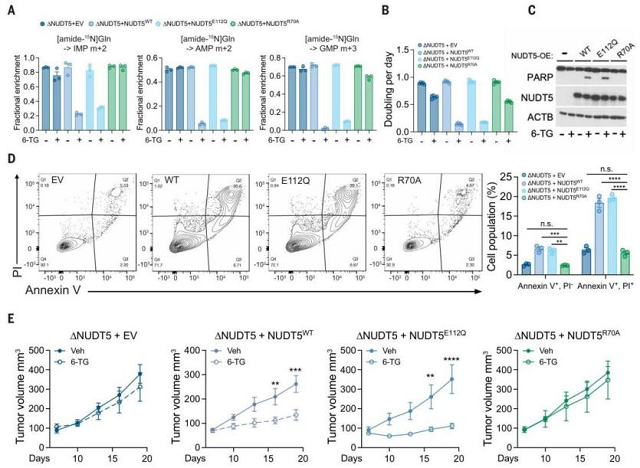
图4
研究小结
本研究通过整合代谢组学与同位素示踪技术,首次系统阐明NUDT5在嘌呤代谢中的非酶调控功能,揭示其作为DNPB与补救合成之间分子开关的新机制,即与PPAT互作调控嘌呤体动态,从而抑制DNPB并决定硫嘌呤药物敏感性。该发现不仅深化了对嘌呤代谢平衡的理解,也为硫嘌呤个体化治疗提供了潜在的生物标志物和干预靶点。
在本研究中,多种质谱技术整合同位素示踪技术协同应用于代谢组学中,共同构建了从蛋白质表达变化到代谢通量调控的完整证据链。首先,研究团队基于TMT标记的定量蛋白质组学结合高分辨率质谱仪,精确量化了野生型与NUDT5缺失细胞在药物处理后的蛋白表达差异。证实了NUDT5是介导6-TG诱导的细胞凋亡与线粒体功能相关蛋白表达变化所必需,为后续代谢研究奠定了分子表型基础。随后,研究采用稳定同位素示踪结合气相色谱-质谱(GC-MS)与液相色谱-串联质谱(LC-MS/MS),对嘌呤核苷酸中特定¹⁵N4标记体进行高灵敏度、高特异性定量,实现了对从头嘌呤合成通量的精确测量。数据明确显示,6-TG对DNPB的强烈抑制效应严格依赖于NUDT5的存在。该通量数据为NUDT5的核心调控功能提供了最直接的动力学证据。为进一步排除其他可能性并探索下游代谢后果,基于液质技术的靶向代谢组学从代谢物稳态的角度进一步支持了DNPB通量受NUDT5调控的结论。
综上所述,代谢组学与同位素示踪技术的联合应用,为证实NUDT5通过蛋白互作调控嘌呤体动态与DNPB通量、进而决定硫嘌呤药物敏感性的创新机制,提供了有力的实验支持。二者在代谢物稳态检测与代谢流动态追踪方面具备独特优势,其整合应用有助于全面、动态地解析生物代谢过程,为精准医学与药物机制研究提供可靠的技术路径。
科似海生物检测服务
科似海生物长期致力于突破代谢质谱检测的技术瓶颈,专注于提供定制化的代谢研究解决方案。公司开发了多项核心技术,涵盖超微量样本代谢物检测、稳定同位素代谢示踪以及全景覆盖的代谢组学与脂质组学常规分析,致力于为客户提供可靠、精准的科学数据。
作为一家专注于攻克技术难点的研发与检测服务企业,科似海生物在组织、胚胎、细胞、培养基等微量及珍贵样本的小分子代谢组学和脂质组学检测方面积累了丰富经验,致力于为更多科研团队提供精准、可靠的技术服务,让“难检测、测不准”的微量样本,不再成为科研路上的障碍。如果您也面临微量/珍贵样本的代谢检测难题,欢迎联系科似海——我们期待成为您科研路上的“技术队友”,共同推动更多科学发现!
【参考文献】
[1] Wu Z, Nguyen PT, Sondhi V, et al. NUDT5 regulates purine metabolism and thiopurine sensitivity by interacting with PPAT. Science. 2025;390(6778):1134-1142. doi:10.1126/science.adx9717