脂质组学是生命科学最具挑战性的研究领域之一。相较于基因或蛋白质,脂质不仅种类超千种,还存在碳链长度、不饱和度、双键位置等复杂异构性,这为其检测与准确定量带来了巨大困难。
大脑作为人体脂质最富集的器官之一,其脂质稳态更是神经功能的“生命线”。从罕见的神经元蜡样脂褐质沉积症,到常见的阿尔茨海默病、帕金森病,诸多神经退行性疾病都与脂质代谢紊乱相关;甚至衰老、炎症、睡眠节律紊乱等也会打破脑内脂质平衡。然而,脑脂质研究的复杂性远超其他组织:脑组织具有显著的细胞类型与脑区特异性,例如神经元、星形胶质细胞、小胶质细胞之间,以及灰质与白质之间的脂质组成差异明显。同时,样本的年龄、饮食条件和死亡后间隔时间等因素也会显著影响脂质稳态,使得研究人员在识别疾病相关的原发性脂质代谢异常时面临严峻挑战。
尽管转录组与蛋白质组学已建立标准化的数据库,神经脂质组学目前仍缺乏统一平台与比对体系,这一现状严重限制了跨疾病、跨模型的脂质代谢整合研究,也制约了该领域的发展进程。
2025年9月22日,荷兰阿姆斯特丹自由大学神经基因组学与认知研究中心团队与莱顿大学医学中心团队合作,在《Nature Metabolism》杂志上发表题为“The Neurolipid Atlas: a lipidomics resource for neurodegenerative diseases”的文章,构建了开放共享的神经脂质数据平台Neurolipid Atlas(https://neurolipidatlas.com)。该数据平台系统性的整合了人类诱导多能干细胞(iPSC)来源的神经元、星形胶质细胞和小胶质细胞的脂质组学数据和多种神经疾病模型与人/鼠脑组织脂质组数据,为神经退行性疾病研究提供了 “跨场景、可对比” 的核心工具,彻底打破了长期存在的 “数据孤岛” 困境 [1]。

研究结果
PART-01
iPSC来源脑细胞的脂质图谱:体外模型
精准复刻体内脂质特征
研究团队首先建立了可定量超1000种脂质的标准化iPSC脂质组学技术。将 iPSC 分化为神经元(iNeurons)、星形胶质细胞(iAstrocytes)、小胶质细胞(iMicroglia)三类核心脑细胞。结果显示,三类细胞的脂质组成差异显著且高度贴合体内状态:iNeurons 富含磷脂酰胆碱(PC)与磷脂酰乙醇胺(PE);iMicroglia 富含鞘磷脂(SM)与磷脂酰丝氨酸(PS);而iAstrocytes 含有最高的胆固醇酯(CE)水平,且与小鼠原代脑细胞的脂质分布高度一致。这意味着 iPSC 衍生细胞不仅在转录、蛋白层面模拟脑细胞,更在脂质层面实现 “精准复刻”,为神经疾病体外模型研究提供了可靠基础。
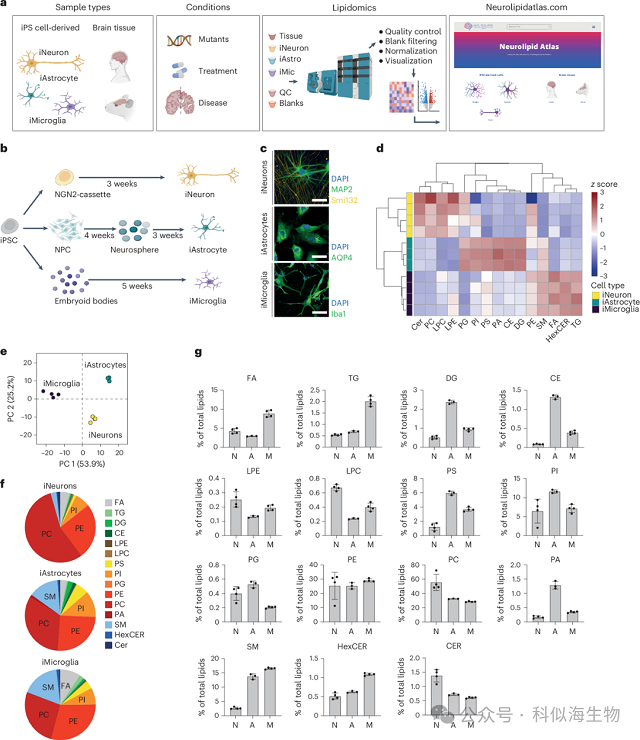
图1
PART-02
人类阿尔茨海默病脑组织的脂质异常:
胆固醇酯积累是核心脂质特征
针对33例人脑样本(20例阿尔兹海默症患者,13例对照),研究分析了额叶灰质、白质和小脑的脂质组成。发现两大规律:(1)不同脑区脂质组成具有明显差异,例如白质区域富含鞘磷脂(SM)和神经酰胺(CERs),灰质则以磷脂和中性脂(甘油三脂TG和胆固醇酯CE)为主;(2)阿尔兹海默症患者样本在额叶灰质与白质中胆固醇酯(CE)显著升高,并伴有甘油三酯(TG)、二酰甘油(DG)升高,并且乳糖基神经酰胺(LacCER)在阿尔兹海默症患者的白质中含量升高。以上结果表明中性脂(尤其是CE)的积累,是阿尔兹海默症患者脑组织的核心脂质学特征,提示胆固醇代谢紊乱与AD病理过程密切相关。
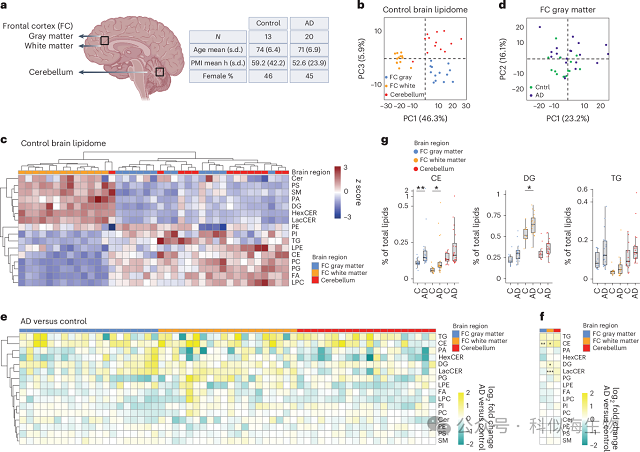
图2
PART-03
ApoE4:驱动星形胶质细胞脂质
异常的 “关键推手”
ApoE 是脑内主要胆固醇载体,其中 ApoE4 等位基因是阿尔茨海默病最强的遗传风险因子。为探究其与脂质异常的关系,研究对比了同基因背景的 ApoE3/3 与 ApoE4/4 星形胶质细胞:ApoE4 型细胞中,胆固醇酯(CE)、甘油三酯(TG)显著积累,脂滴数量明显增多;与之相反,鞘磷脂(SM)含量显著下降。这表明 ApoE4 通过促进胆固醇酯化、增加中性脂储存,直接改变星形胶质细胞的脂质代谢,成为 AD 脂质异常的 “核心驱动分子”。
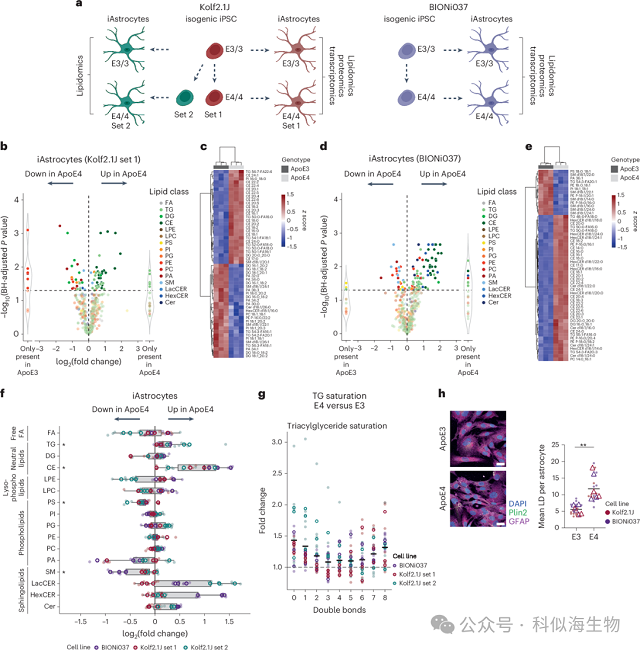
图3
PART-04
ApoE4抑制星形胶质细胞的
免疫与抗原呈递功能
上述结果表明,ApoE4等位型可显著促进人源星形胶质细胞(iAstrocytes)中胆固醇酯(CE)的积累。为进一步解析这一代谢变化的功能后果,研究团队对两对同基因背景的iAstrocyte系列(BIONi037 与 Kolf2.1J)开展了蛋白质组学与转录组学联合分析。其中,蛋白质组与脂质组测定基于同一批细胞样本,以确保多组学结果的可整合性与一致性。综合分析显示,ApoE4 型星形胶质细胞中ApoE蛋白表达下调,同时细胞外基质重塑与细胞黏附相关通路上调;相反,干扰素信号通路、MHC I抗原呈递及免疫蛋白酶体相关通路均显著下调。多种实验验证(包括Western blot、流式细胞术及免疫荧光)一致证实人类白细胞抗原(HLA)以及抗原加工转运蛋白TAP1/TAP2的表达水平明显降低。转录组分析结果与蛋白质组变化相吻合,进一步支持ApoE4通过抑制干扰素依赖的免疫反应途径削弱星形胶质细胞的免疫功能,揭示了胆固醇代谢异常与免疫调控受损之间的分子联系。
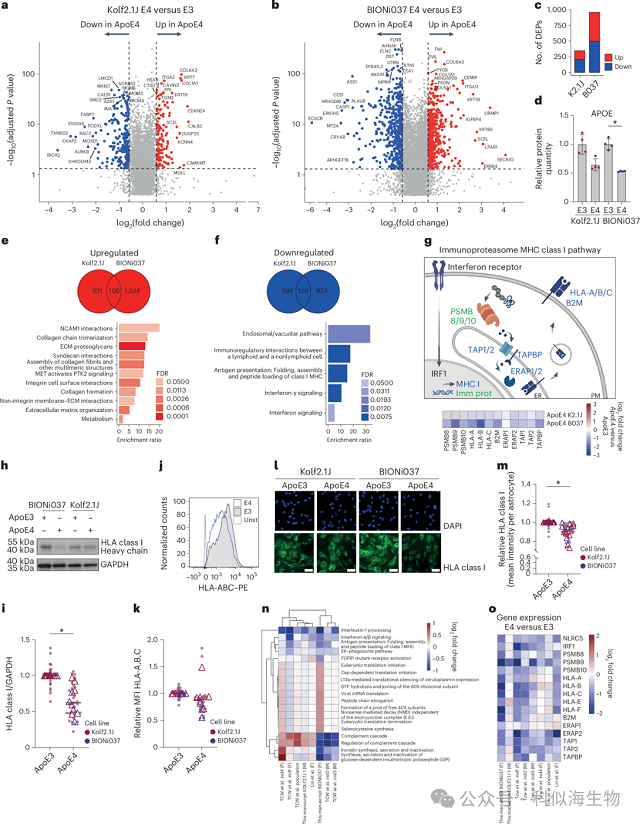
图4
PART-05
反应性星形胶质细胞与 ApoE4 细胞
呈相反的脂质-免疫表型
尽管阿尔茨海默病晚期常伴随星形胶质细胞活化(astrogliosis)和免疫增强,但研究结果却发现,ApoE4 型星形胶质细胞中的干扰素依赖性通路反而显著下调。为进一步阐明这种抑制性表型与脂质代谢变化之间的关系,作者对经TNF、IL-1α和C1q刺激诱导的反应性星形胶质细胞(Reactive iAstrocytes)进行了多组学分析。结果显示在反应性星形胶质细胞中,CE和TG水平显著下降,而饱和磷脂与MHC I抗原呈递、干扰素信号及免疫蛋白酶体通路显著上调;与之相反,ApoE4 型细胞表现为CE和TG积累并伴随这些免疫通路的下调。值得注意的是,即便在ApoE4型细胞中,强烈的促炎刺激(TNF、IL-1α、C1q)仍可降低CE和TG并恢复MHC I水平,这表明外源性炎症可逆转 ApoE4 诱导的免疫抑制表型。总的来说,反应性星形胶质细胞与 ApoE4 型星形胶质细胞展现出相反的“脂质-免疫耦合模式”:前者表现为脂质动员与免疫激活,后者则表现为脂质堆积与免疫抑制。这一“镜像关系”揭示了胆固醇代谢与免疫反应之间的动态平衡,是理解神经退行性病变中代谢-免疫互作的重要机制。
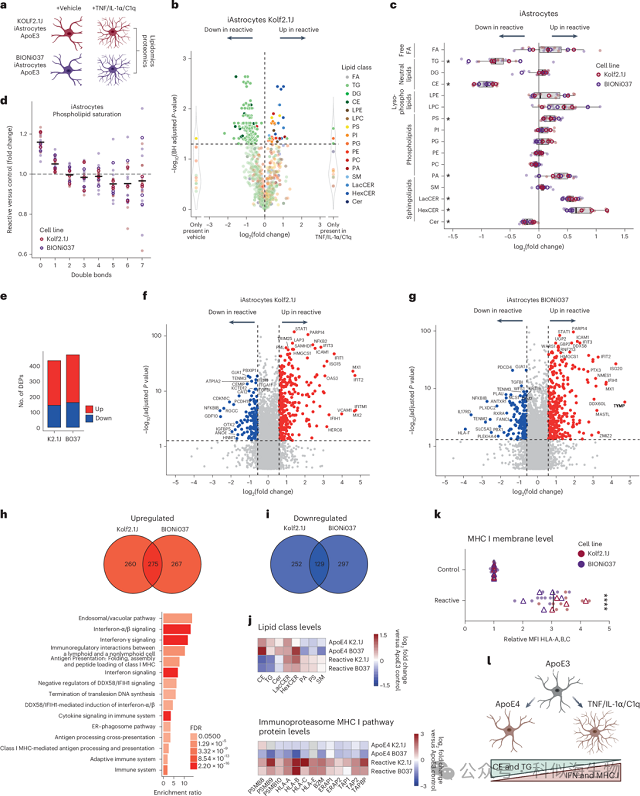
图5
PART-06
胆固醇代谢直接调控星形胶质细胞
的免疫反应
基于反应性星形胶质细胞中CE水平下降而ApoE4型细胞中CE水平上升,研究团队假设胆固醇代谢的变化可能直接影响免疫表型。为验证胆固醇是否调控人源星形胶质细胞的免疫反应,研究者对ApoE3型细胞添加胆固醇进行处理。结果显示:(1)胆固醇处理显著增强了MHC I抗原呈递和IL-6分泌;(2)进一步抑制ACAT(胆固醇酰基转移酶)产生的CE后,IL-6的分泌得到了增强,表明CE的形成缓解了胆固醇引起的免疫反应;(3)此外,外源性胆固醇还促进了干扰素调控因子IRF1和HLA-B的上调,提示胆固醇对这些免疫通路的影响可能是通过转录调控介导的。胆固醇处理也显著提高了饱和磷脂水平,这是星形胶质细胞活化的标志。另一方面,他汀类药物(如阿托伐他汀)通过降低胆固醇水平,抑制了反应性星形胶质细胞中的MHC I上调和IL-6分泌。最后,在ApoE4型星形胶质细胞中添加胆固醇可恢复MHC I表达和IL-6分泌,进一步支持胆固醇在免疫调控中的关键作用。
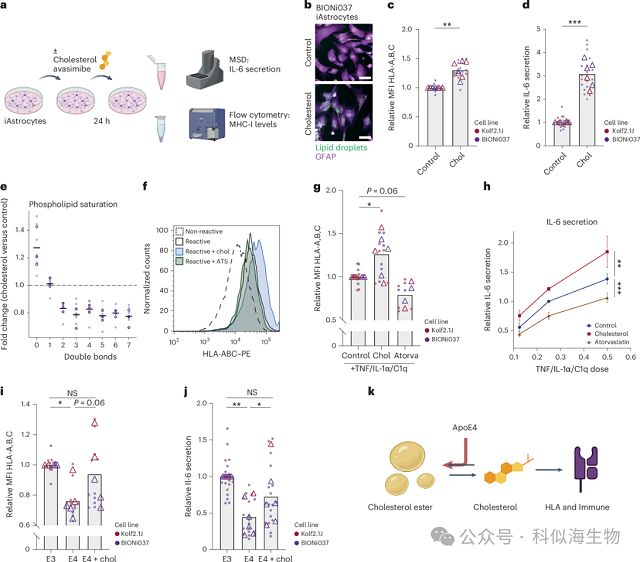
图6
最后研究团队展示了他们构建的首个系统化的神经脂质组学数据平台——Neurolipid Atlas。该资源平台包含两大模块:
(1)iPSC 衍生脑细胞数据:涵盖神经元、星形胶质细胞、小胶质细胞,采用标准化流程定量超 1000 种脂质,为体外疾病模型研究提供 “基准参考”;
(2)人类 / 小鼠脑组织数据:覆盖阿尔茨海默病(AD)、帕金森病(PD)、肌萎缩侧索硬化(ALS)、额颞叶痴呆(FTD)等多种神经退行性疾病,包含不同脑区、不同疾病阶段的样本,助力 “体内病理 - 脂质异常” 关联分析。Neurolipid Atlas 的建立,解决研究行业 “核心痛点”
①打破 “数据孤岛”:统一数据格式与分析标准,支持跨疾病、跨模型、跨实验室的数据比对,避免 “各做各的,无法整合” 的困境;
②降低研究门槛:开放共享的模式让中小实验室无需重复构建脂质组学平台,直接基于已有数据开展挖掘,节省时间与成本;
③提供 “从分子到疾病” 的视角:将脂质数据与细胞功能、疾病病理关联,帮助科研人员快速定位 “关键脂质分子”,缩短机制研究周期。
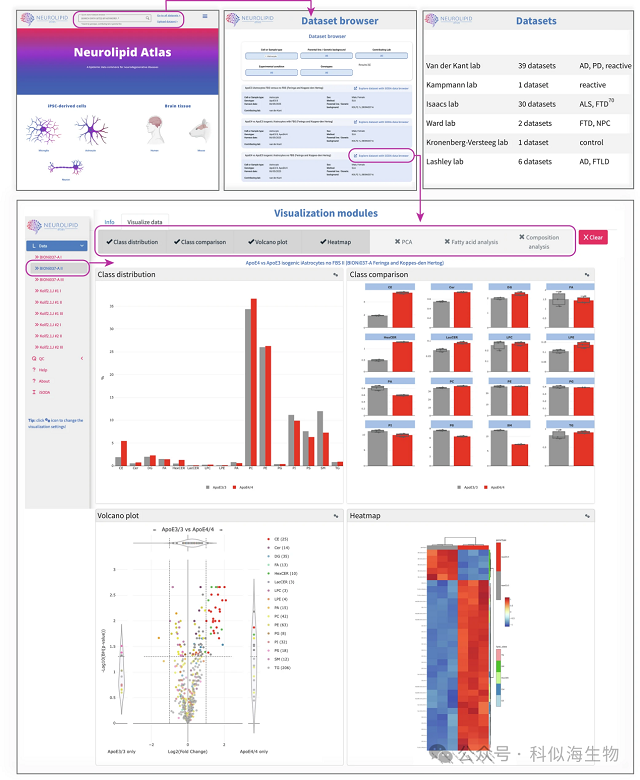
图7
科似海生物检测服务
科似海生物专注于精准脂质组学技术服务,依托自主研发的高通量核心分析系统,构建了从脂质谱解析、代谢调控网络构建到生物标志物发现的一体化服务体系。我们的系统兼具超高特异性与极致灵敏度。在技术层面,我们创新性地突破了传统脂质标准品有限的技术瓶颈,确保了对数千种脂质的准确标注鉴定,从源头杜绝假阳性与误判问题;同时,实现了微量样品量下的高灵敏度、深度检测。目前,其检测范围已全面覆盖双酰基甘油磷脂、溶血磷脂、神经酰胺脂质、磷酸鞘脂类、甘油脂及胆固醇等数千余类关键脂质。针对心磷脂(cardiolipin)、双单酰甘油磷酸酯(BMP,溶酶体脂质)等高难度、复杂脂质,我们进行了针对性的技术创新优化,确保精准定量,全面满足多样化的研究需求。
科似海生物的精准脂质组学技术服务面向肿瘤、代谢性疾病、神经退行性病变等前沿研究领域,提供从检测方案设计到数据分析的定制化服务。我们始终秉承 “解析生命脂质语言,赋能精准医学发展”的理念,将技术专业性与数据准确性贯穿于服务全流程。科似海生物将持续深化与高校、医院及药企的产学研合作,通过技术输出、联合研发,加速推动脂质组学从基础机制探究向临床应用转化,为精准医学发展注入持久且强劲的动力。
【参考文献】
[1] Feringa, F.M., Koppes-den Hertog, S.J., Wang, L.Y. et al. The Neurolipid Atlas: a lipidomics resource for neurodegenerative diseases. Nat Metab (2025).