在生命的微观图景中,细胞犹如一座精密运转的城市,溶酶体则扮演着“垃圾回收站”的角色,负责降解并回收细胞内外的各类大分子物质。一种名为 Bis (monoacylglycerol) phosphate(BMP)的磷脂分子,正是维系这座 “回收站” 高效运转的关键 “清道夫”。随着高分辨质谱技术的发展,BMP 在溶酶体功能中的核心作用逐渐明晰,如今已成为溶酶体贮积症、神经退行性疾病及衰老研究的重要生物标志物。
本文带您简单梳理 BMP 的基础特性与生物功能,解析其检测技术难点并提供针对性的解决方案如何通过精准质谱检测助力BMP在生物医学领域的研究。
一、BMP:一种“反常规”的溶酶体磷脂
BMP是一种结构独特的磷脂,其名称“Bis(monoacylglycerol)phosphate”来源于其化学构成——由两个单酰基甘油分子通过一个磷酸基团连接而成。与常见磷脂不同,BMP的两条脂肪酸链分别位于两个独立的甘油骨架上,其磷酸二酯部分仅连接在甘油的 sn-1 和 sn-1' 位,而非通常的 sn-3 与 sn-3' 位;而脂肪酸则可能酯化在 sn-3/3' 位置上。这种特殊排列使其具备一系列独特的空间构象(图1)。这种“反常规”结构,赋予BMP 三大关键理化性质:在细胞膜中呈现强负电性;促进膜结构弯曲;表现出极高的化学稳定性。
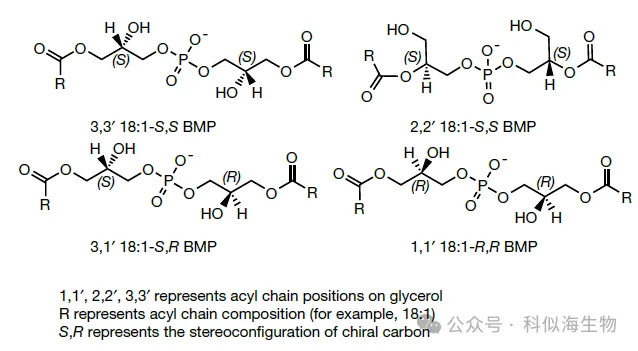
(图1)【4】
从细胞分布来看,BMP并非广泛分布于各类膜结构中,而是高度富集在溶酶体,是公认的“溶酶体特征性脂质”。其核心功能直接服务于溶酶体的“清理职责”:一方面能够显著增强多种降解酶(如鞘脂酶)的活性,加速鞘脂等复杂脂质的水解过程;另一方面维持溶酶体膜结构稳定、保障脂质降解产物的高效回收利用。
二、BMP与人类健康:小分子撬动大领域,近年研究突破不断
尽管BMP在细胞总脂质中的占比极低(<1%),但其功能异常直接导致溶酶体 “清理失灵”,引发细胞内脂质堆积,进而诱发一系列疾病。自1966年BMP被首次鉴定以来[1],其机制研究长期停滞,直到近年才迎来多项里程碑式突破,明确了它与神经退行性疾病、溶酶体贮积症、衰老等领域的紧密关联。
1. 2023年《Science》:解锁BMP合成关键酶,关联神经疾病
该研究首次发现,巴顿病(一种遗传性神经系统疾病)相关基因 CLN5 的编码蛋白,正是 BMP 合成通路中的关键酶 [2]。具体而言,CLN5 通过催化 “转酰基反应” 推动 BMP 合成;若 CLN5 发生突变,不仅会直接抑制 BMP 生成,还会导致溶酶体功能紊乱、神经节苷脂(一种神经细胞关键脂质)异常堆积。
这一发现首次建立了 “CLN5 酶活性→BMP 合成→溶酶体功能→神经病理” 的分子链条,为阿尔茨海默病、巴顿病等神经退行性疾病的靶向治疗提供了核心理论依据。
2. 2024 年《Cell》:揭示 BMP 构型调控酶,深化脑与免疫关联
研究团队进一步发现,磷脂酶 PLD3 和 PLD4 是调控 BMP 不同构型(如 S,S-BMP)动态转换的关键分子 [3]。实验证实:缺失 PLD3 或 PLD4 会显著降低细胞及特定组织中的 BMP 水平(PLD3 高表达于大脑,PLD4 高表达于脾脏)。上述缺失会引发神经节苷脂沉积、溶酶体功能异常。更重要的是,PLD3 催化活性降低的突变体,已被证实与阿尔茨海默病的发病风险直接相关。这一成果不仅完善了 BMP 的调控网络,还为 “脑 - 免疫组织” 中 BMP 功能的协同研究提供了新方向。
3. 2025 年《Nature》:定位 BMP 降解酶,开启溶酶体病治疗新路径
今年 5 月发表的研究明确,磷脂酶 PLA2G15 是负责 BMP 降解的关键水解酶 [4]。在尼曼 - 匹克病 C 型(一种罕见溶酶体贮积症)模型小鼠中,抑制 PLA2G15 可有效促进 BMP 在体内累积,进而显著延长小鼠的存活寿命。这一发现首次验证了 “靶向 BMP 代谢通路” 治疗溶酶体贮积症的可行性,为罕见病治疗提供了全新的潜在靶点。
此外,2024年同期背靠背发表于《Nature Aging》的两项研究证实BMP在衰老的小鼠和人类组织中存在普遍累积[5, 6]。此外,后续综述研究进一步指出,BMP 异常还与癌症、病毒感染及更多神经退行性疾病相关 [7](图 2)—— 这意味着 BMP 已成为连接 “衰老 - 疾病” 研究的重要分子标志物。
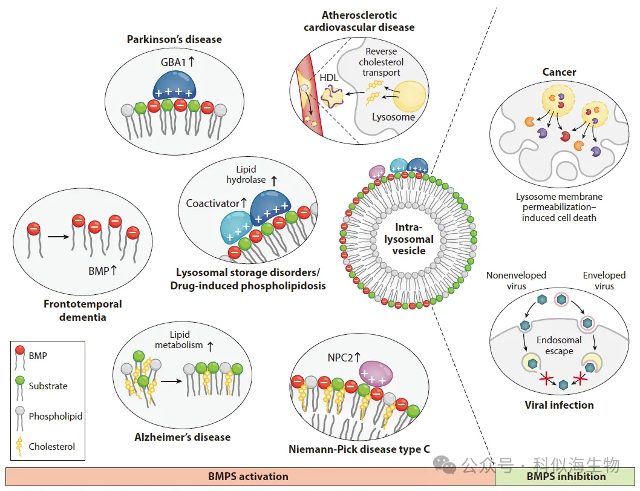
(图2)【7】
三、BMP研究的“拦路虎”: 三大检测技术难点
尽管 BMP 的研究价值日益凸显,但其检测技术长期面临三大核心挑战,制约了研究与应用的推进。
1.与同分异构体PG 的 “鉴别难题”
BMP与同分异构体磷脂酰甘油(PG)在常规质谱检测条件下难以鉴别。为实现准确鉴定,需依赖正离子模式下BMP特有的特征离子碎片进行定性,并在此基础上建立针对性的定量方法,方可实现对样品中BMP含量的精确测定。
2.BMP 自身异构体的 “分离难题”
即使是同一种BMP分子也存在多种异构体(图1),而这些异构体在极性、色谱保留时间差异甚微,导致其在常规色谱条件下无法有效分离,进而影响定量的准确性,甚至引发误判。目前,有研究尝试采用化学衍生化策略以增强异构体间的分离度,然而该方法本身存在反应效率不一、引入副反应等问题,难以广泛应用。
3.低含量与高复杂性的“同步检测难题”
BMP在细胞总脂质中占比不足1%,属于典型的“微量脂质”。与此同时,BMP并非单一分子,而是一个由不同脂肪酸链组合与空间异构体所构成的复杂家族。要在低丰度背景下,对这个 “家族” 的每个成员实现精准定性与定量,对分析方法的灵敏度、分辨率和通量提出了极高难度的挑战。
四、精准检测破局:从 “单一分子” 到 “脂链网络” 的系统解决方案重塑商务生态
针对 BMP 检测的三大核心难点,科似海生物已建立全套优化技术体系,为不同领域用户提供专业支撑:
攻克同分异构体鉴别:通过优化液相色谱(LC)分离条件,在常规质谱平台上实现了 BMP 与 PG 的基线分离(即信号完全不重叠),并建立独立定量方法,彻底解决 “鉴别难” 问题;
保障微量精准定量:依托高灵敏度质谱平台,可稳定检测低至e4数量级的细胞样本BMP 的含量;
拓展系统研究视角:不仅聚焦 BMP 本身,还可同步对其调控的关键脂质(如鞘脂、胆固醇、神经节苷脂)进行高覆盖、高精度脂质组学分析—— 帮助科研人员从 “单一分子功能” 延伸至 “脂质调控网络”,为疾病机制研究、药物靶点筛选提供更全面的数据支撑。
科似海生物检测服务
科似海生物长期致力于突破代谢质谱检测的技术瓶颈,专注于提供定制化的代谢研究解决方案。公司开发了多项核心技术,涵盖超微量样本代谢物检测、稳定同位素代谢示踪以及全景覆盖的代谢组学与脂质组学常规分析,致力于为客户提供可靠、精准的科学数据。
作为一家专注于攻克技术难点的研发与检测服务企业,科似海生物在组织、胚胎、细胞、培养基等微量及珍贵样本的小分子代谢组学和脂质组学检测方面积累了丰富经验,致力于为更多科研团队提供精准、可靠的技术服务,让“难检测、测不准”的微量样本,不再成为科研路上的障碍。如果您也面临微量/珍贵样本的代谢检测难题,欢迎联系科似海——我们期待成为您科研路上的“技术队友”,共同推动更多科学发现!
【参考文献】
[1] Body D.R., Gray G.M. The isolation and characterisation of phosphatidylglycerol and a structural isomer from pig lung. Chem. Phys. Lipids, 1967; 1(3): 254-263. doi:10.1016/0009-3084(67)90032-1
[2] Medoh UN, Hims A, Chen JY, et al. The Batten disease gene product CLN5 is the lysosomal bis(monoacylglycero)phosphate synthase. Science. 2023;381(6663):1182-1189. doi:10.1126/science.adg9288
[3] Singh S, Dransfeld UE, Ambaw YA, Lopez-Scarim J, Farese RV Jr, Walther TC. PLD3 and PLD4 synthesize S,S-BMP, a key phospholipid enabling lipid degradation in lysosomes. Cell. 2024;187(24):6820-6834.e24. doi:10.1016/j.cell.2024.09.036
[4] Nyame K, Xiong J, Alsohybe HN, et al. PLA2G15 is a BMP hydrolase and its targeting ameliorates lysosomal disease. Nature. 2025;642(8067):474-483. doi:10.1038/s41586-025-08942-y
[5] Tsugawa H, Ishihara T, Ogasa K, et al. A lipidome landscape of aging in mice. Nat Aging. 2024;4(5):709-726. doi:10.1038/s43587-024-00610-6
[6] Janssens GE, Molenaars M, Herzog K, et al. A conserved complex lipid signature marks human muscle aging and responds to short-term exercise. Nat Aging. 2024;4(5):681-693. doi:10.1038/s43587-024-00595-2
[7] Medoh, U. N., & Abu-Remaileh, M. (2024). The Bis(monoacylglycero)-phosphate Hypothesis: From Lysosomal Function to Therapeutic Avenues. Annual review of biochemistry, 93(1), 447–469. https://doi.org/10.1146/annurev-biochem-092823-113814